题目内容
1.下述实验能达到预期目的是( )| 编号 | 实验内容 | 实验目的或结论 |
| A | 将少量AgNO3溶液滴加到含有Cl-、CrO42-的溶液 | 确定Ksp(AgCl)、Ksp(Ag2CrO4)的相对大小 |
| B | 将C2H5OH与浓H2SO4在蒸馏烧瓶中混合后加热至170℃,将从瓶内逸出的物质依次通过NaOH溶液、溴水 | 检验有无乙烯生成 |
| C | 将铁与稀硝酸混合,充分反应后再向溶液中加入KSCN溶液 | 探究铁能否被氧化成Fe3+ |
| D | 向FeBr2溶液加入少量氯水,观察溶液是否变黄色 | 确定Fe2+与Br-还原性强弱 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.需要c(Ag+)越小,先生成沉淀;
B.NaOH溶液可除去杂质,乙烯与溴水发生加成反应;
C.若Fe过量生成硝酸亚铁;
D.加入少量氯水,只氧化亚铁离子.
解答 解:A.需要c(Ag+)越小,先生成沉淀,因难溶电解质的类型不同,不能直接比较Ksp,故A错误;
B.NaOH溶液可除去杂质,乙烯与溴水发生加成反应,则溴水褪色可检验乙烯生成,故B正确;
C.若Fe过量生成硝酸亚铁,充分反应后再向溶液中加入KSCN溶液,无现象,但Fe可被氧化为Fe3+,该实验不能说明,故C错误;
D.加入少量氯水,只氧化亚铁离子,氯水为浅黄绿色,若生成铁离子为黄色,颜色变化不明显,该实验不能比较Fe2+与Br-还原性强弱,故D错误;
故选B.
点评 本题考查化学实验方案的评价,为高频考点,把握难溶电解质的生成、物质的检验、氧化还原反应为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度中等.

练习册系列答案
 轻巧夺冠周测月考直通中考系列答案
轻巧夺冠周测月考直通中考系列答案
相关题目
11. 一种高能纳米级Fe3S4和镁的二次电池,其工作原理为:Fe3S4+4Mg$?_{充电}^{放电}$3Fe+4MgS,装置如图所示.下列说法不正确的是( )
一种高能纳米级Fe3S4和镁的二次电池,其工作原理为:Fe3S4+4Mg$?_{充电}^{放电}$3Fe+4MgS,装置如图所示.下列说法不正确的是( )
 一种高能纳米级Fe3S4和镁的二次电池,其工作原理为:Fe3S4+4Mg$?_{充电}^{放电}$3Fe+4MgS,装置如图所示.下列说法不正确的是( )
一种高能纳米级Fe3S4和镁的二次电池,其工作原理为:Fe3S4+4Mg$?_{充电}^{放电}$3Fe+4MgS,装置如图所示.下列说法不正确的是( )| A. | 放电时,电路中转移0.5mol电子则阴离子交换膜上移动0.25mol S2- | |
| B. | 放电时,正极的电极反应式为Fe3S4+8e-=3Fe+4S2- | |
| C. | 充电时,阴极的电极反应式为MgS+2e-=Mg+S2- | |
| D. | 充电时,S2-从阴离子交换膜左侧向右侧迁移 |
12.X、Y、Z、W为短周期元素,且原子序数依次增大.X与W属于同一主族,X2-、Y+离子与氖原子具有相同的电子层结构,Z元素的周期序数等于主族序数.下列说法正确的是( )
| A. | 金属性:Z>Y | |
| B. | 原子半径:W>Z>Y>X | |
| C. | 元素X和Y只能形成一种化合物 | |
| D. | Y、Z、W的最高价氧化物对应的水化物均能相互反应 |
16.下列现象或过程中,不涉及氧化还原反应的是( )
| A. |  酸雨的形成 | B. |  治疗胃酸过多 | C. |  切开的苹果发霉 | D. |  放鞭炮 |
13.两种气态烃的混合物共2.24L(标准状况),完全燃烧后得3.36L(标准状况)二氧化碳和3.6g的水.下列说法中正确的是( )
| A. | 混合气体中一定含有甲烷 | B. | 混合气体中一定含有乙烯 | ||
| C. | 混合气体中可能含有乙炔 | D. | 混合气体一定是由烷烃和烯烃构成 |
10.下列实验操作能达到实验目的是( )
| 实验操作 | 实验目的 | |
| A | 将SO2通入紫色石蕊溶液中 | 证明SO2具有漂白性 |
| B | 取两支试管,分别加入4mL0.01mol•L-1KMnO4溶液,然后向一支试管中加0.1mol•L-1H2C2O4溶液2mL,向另一支试管中加入0.1mol•L-1H2C2O4溶液4mL,记录褪色时间 | 证明草酸浓度越大,反应速率越快 |
| C | 向10mL0.2mol•L-1NaOH溶液中滴入2滴入两滴0.1mol•L-1MgCl2溶液,产生白色沉淀后,再滴加2滴0.1mol•L-1FeCl2溶液,又生成红褐色沉淀 | 证明在相同温度下的溶度积:Ksp[Mg(OH)2]>Ksp[Fe(OH)3] |
| D | 向含酚酞的Na2SO4溶液中加入BaCl2溶液 | 证明Na2SO4溶液中存在水解平衡 |
| A. | A | B. | B | C. | C | D. | D |
20.化学在生产和生活中有着广泛的应用,下列说法不正确的是( )
| A. | 二氧化硫具有漂白性,可广泛用于食品的增白 | |
| B. | 鉴别蚕丝和人造丝(纤维素)的方法之一是灼烧,有烧焦羽毛气味的是蚕丝 | |
| C. | 农村兴建沼气池将秸秆发酵产生沼气,可减少因焚烧带来的环境污染 | |
| D. | 用浸泡过高锰酸钾溶液的硅藻土吸收水果产生的乙烯可达到保鲜的目的 |




 )为原料合成,路线如下(部分反应条件省略):
)为原料合成,路线如下(部分反应条件省略):



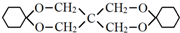 .
. .
.