题目内容
13.脱水环化是合成生物碱类天然产物的重要步骤,某生物碱V合成路线如下: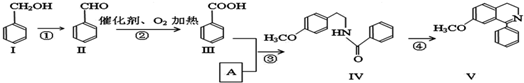
(1)Ⅴ中含氧官能团的名称醚键.
(2)反应①的化学方程式2C6H5CH2OH+O2$→_{△}^{Cu}$2C6H5CHO+2H2O.
(3)下列说法正确的是BD.
A.Ⅰ和Ⅳ均属于芳香烃 B.Ⅱ能发生银镜反应
C.反应③属于酯化反应 D.甲苯和酸性高锰酸钾反应能生成Ⅲ
(4)A的结构简式
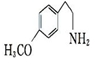 .
.(5)Ⅵ与Ⅰ互为同分异构体,Ⅵ遇FeCl3发生显色反应,其苯环上的一氯代物只有2种.写出满足上述条件的Ⅵ的结构简式
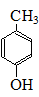 .
.
分析 (1)根据结构简式确定官能团;
(2)反应①为苯甲醇的催化氧化反应;
(3)A.化合物Ⅰ、Ⅴ含有C和H以外的元素,不属于烃类;
B.化合物Ⅱ分子中含-CHO,具有醛的性质;
C.反应③的产物中形成 ,不含酯基;
,不含酯基;
D.甲苯可被氧化生成苯甲酸;
(4)由反应③的产物IV逆向分析,应从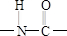 之间断键,故A是
之间断键,故A是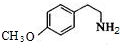 ;
;
(5)化合物Ⅵ与化合物I互为同分异构体,Ⅵ遇 FeCl3发生显色反应,含有酚羟基,另外取代基为甲基,其苯环上的一氯代物只有2种,则酚羟基与甲基处于对位.
解答 解:(1)由结构简式可知Ⅴ中含氧官能团为醚键,故答案为:醚键;
(2)反应①为苯甲醇的催化氧化反应,方程式为2C6H5CH2OH+O2$→_{△}^{Cu}$2C6H5CHO+2H2O,故答案为:2C6H5CH2OH+O2$→_{△}^{Cu}$2C6H5CHO+2H2O;
(3)A.化合物Ⅰ、Ⅴ含有C和H以外的元素,不属于烃类,属于烃的衍生物,故A错误;
B.化合物Ⅱ分子中含-CHO,具有醛的性质,能发生银镜反应,故B正确;
C.反应③的产物中形成 ,不含酯基,不属于酯化反应,故C错误;
,不含酯基,不属于酯化反应,故C错误;
D.甲苯可被氧化生成苯甲酸,故D正确.
故答案为:BD;
(4)由反应③的产物IV逆向分析,应从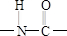 之间断键,故A是
之间断键,故A是 ,故答案为:
,故答案为: ;
;
(5)化合物Ⅵ与化合物I互为同分异构体,Ⅵ遇FeCl3发生显色反应,含有酚羟基,另外取代基为甲基,其苯环上的一氯代物只有2种,则酚羟基与甲基处于对位,Ⅵ的结构简式为 ,故答案为:
,故答案为:
点评 本题考查有机物的推断与合成、官能团的结构与性质、同分异构体书写、有机反应方程式等,充分利用有机物的结构分析解答,是对有机化学的综合考查,侧重考查学生分析推理与知识迁移运用能力考查,难度较大.

练习册系列答案
相关题目
3.能证明苯酚具有弱酸性的实验是( )
| A. | 加入浓溴水生成白色沉淀 | |
| B. | 苯酚钠溶液中通入CO2后,溶液由澄清变浑浊 | |
| C. | 浑浊的苯酚加热后变澄清 | |
| D. | 苯酚的水溶液中加NaOH溶液,生成苯酚钠 |
1.将AgNO3、Na2SO4、BaCl2三种物质按物质的量为2:1:1的比例混合后溶于足量水中,最终溶液中大量存在的离子是( )
| A. | Ba2+和NO3- | B. | Na+和Cl- | C. | Ag+和SO42- | D. | Na+和NO3- |
8.下列有关物质分类或归类正确的是( )
①混合物:盐酸、漂白粉、水玻璃、水银
②化合物:CaCl2、NaOH、HCl、HD
③电解质:明矾、石膏、冰醋酸、氯化银
④同素异形体:C60、C70、金刚石、石墨
⑤放热反应:盐酸与氢氧化钠、碳酸钙高温分解、甲烷燃烧.
①混合物:盐酸、漂白粉、水玻璃、水银
②化合物:CaCl2、NaOH、HCl、HD
③电解质:明矾、石膏、冰醋酸、氯化银
④同素异形体:C60、C70、金刚石、石墨
⑤放热反应:盐酸与氢氧化钠、碳酸钙高温分解、甲烷燃烧.
| A. | ③④ | B. | ①③④ | C. | ②③④ | D. | ④⑤ |
5.已知25℃、101kPa条件下:4Al(s)+3O2(g)═2Al2O3(s),△H=-2834.9kJ/mol;4Al(s)+2O3(g)═2Al2O3(s),△H=-3119.1kJ/mol.由此得出的正确结论是( )
| A. | 等质量的O2比O3能量低,由O2变O3为放热 | |
| B. | O3比O2稳定,由O2变O3为放热 | |
| C. | 等质量的O2比O3能量高,由O2变O3为吸热 | |
| D. | O2比O3稳定,由O2变O3为吸热 |
3.反应3S+6NaOH=2Na2S+Na2SO3+3H2O中,氧化剂与还原剂的质量比为( )
| A. | 1:3 | B. | 2:1 | C. | 3:1 | D. | 1:2 |