题目内容
6.下列判断正确的是( )| A. | HF、HCl、HBr、HI的热稳定性和还原性依次减弱 | |
| B. | 第三周期非金属元素含氧酸的酸性从左到右依次增强 | |
| C. | 根据金属活动性顺序表,氧化性:Fe3+>Cu2+>Mg2+ | |
| D. | 碱性:NaOH>Mg(OH)2>Al(OH)3 |
分析 A.非金属性越强,对应氢化物越稳定,对应阴离子的还原性越弱;
B.第三周期从左向右非金属性增强,对应最高价氧化物的水化物酸性增强;
B.活动性顺序中金属性越强,对应金属离子的氧化性越弱;
C.金属性越强,对应最高价氧化物的水化物碱性越强.
解答 解:A.非金属性F>Cl>Br>I,则HF、HCl、HBr、HI的热稳定性依次减弱,还原性增强,故A错误;
B.第三周期中从Si→Cl非金属性增强,最高价氧化物的水化物酸性增强,不是最高价含氧酸无此规律,故B错误;
C.由金属性活泼性及Cu与氯化铁的反应可知,氧化性:Fe3+>Cu2+>Mg2+,故C正确;
D.金属性Na>Mg>Al,碱性:NaOH>Mg(OH)2>Al(OH)3,故D正确;
故选CD.
点评 本题考查元素周期律和周期表的应用,为高频考点,把握元素的位置、性质、元素周期律为解答的关键,侧重分析与应用能力的考查,注意规律性知识的应用,题目难度不大.

练习册系列答案
相关题目
17.某烃分子中有一个由碳碳单键构成的六元环,有一个碳碳双键,还有一个碳碳叁键,则能满足上述条件的烃的分子式可能是( )
| A. | C8H8 | B. | C10H16 | C. | C14H22 | D. | C12H22 |
14.下列说法中错误的是( )
| A. | 食盐可作为调味剂、食品防腐剂,还可用于调节体液电解质平衡 | |
| B. | 碘是人体必需的影响智力发育的微量元素,但也不能摄入过多 | |
| C. | 油脂是高能量营养物质,肥胖者不能食用 | |
| D. | 面粉中添加适量的小苏打后做成馒头,既无酸味又疏松可口 |
1.下列各组物质中,化学键全部为共价键的是( )
| A. | NH4Cl、CO2、HCl | B. | O2、KF、SO2 | C. | HCl、CH3COOH、CH4 | D. | Na2O2、N2、H2O |
11.一定条件下,可逆反应N2+3H2═2NH3(放热反应) 达到平衡后,只改变一个条件,下列叙述错误的是( )
| A. | 加催化剂,v正、v逆 都发生变化,且变化的倍数相等 | |
| B. | 加压,v正、v逆 都增大,且v正 增大的倍数大于V逆增大的倍数 | |
| C. | 增大氮气的浓度,H2的平衡转化率增大 | |
| D. | 降温,v正、v逆 都减小,且v正 减小的倍数大于v逆减小的倍数 |
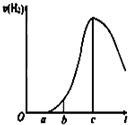 某化学小组进行了关于“活泼金属与酸反应”的实验,得出了一些有趣的想法,请你帮助他们,完成一些判断.将5.4g铝片投入500mL 0.5mol•L-1的硫酸溶液中,如图为反应产氢速率与反应时间的关系图.
某化学小组进行了关于“活泼金属与酸反应”的实验,得出了一些有趣的想法,请你帮助他们,完成一些判断.将5.4g铝片投入500mL 0.5mol•L-1的硫酸溶液中,如图为反应产氢速率与反应时间的关系图. 和
和