题目内容
下列方程式书写不正确的是( )
| A、NaHS水解:HS-+H2O?H2S+OH- |
| B、氢氧化钡溶于水电离:Ba(OH)2═Ba2++2OH- |
| C、醋酸溶于水电离:CH3COOH?CH3COO-+H+ |
| D、碳酸钠水解:CO32-+2H2O?2OH-+H2CO3 |
考点:离子方程式的书写
专题:离子反应专题
分析:A.水解生成氢硫酸和氢氧根离子;
B.强碱,完全电离;
C.醋酸为弱酸,存在电离平衡;
D.碳酸根离子水解分步进行,以第一步为主.
B.强碱,完全电离;
C.醋酸为弱酸,存在电离平衡;
D.碳酸根离子水解分步进行,以第一步为主.
解答:
解:A.NaHS水解的离子反应为HS-+H2O?H2S+OH-,故A正确;
B.氢氧化钡溶于水电离方程式为Ba(OH)2═Ba2++2OH-,故B正确;
C.醋酸溶于水电离方程式为CH3COOH?CH3COO-+H+,故C正确;
D.碳酸钠水解离子反应为CO32-+H2O?OH-+HCO3-,故D错误;
故选D.
B.氢氧化钡溶于水电离方程式为Ba(OH)2═Ba2++2OH-,故B正确;
C.醋酸溶于水电离方程式为CH3COOH?CH3COO-+H+,故C正确;
D.碳酸钠水解离子反应为CO32-+H2O?OH-+HCO3-,故D错误;
故选D.
点评:本题考查离子反应的书写,为高考常见题型,把握发生的反应及离子反应的书写方法为解答的关键,侧重水解与电离的离子反应考查,题目难度不大.

练习册系列答案
相关题目
把铜粉放入装有浓氨水的试管中,塞紧试管塞,振荡后发现试管塞越来越紧,且溶液逐渐变为浅黄色(近乎无色)溶液,打开试管塞后,溶液迅速变为蓝色溶液.则下列说法正确的是( )
| A、试管塞越来越紧,是因为反应消耗了大量NH3 |
| B、溶液逐渐变为浅黄色,是因为反应生成了少量的NO2 |
| C、溶液迅速变为蓝色溶液,是因为反应生成了[Cu(H2O)4]2+ |
| D、上述反应原理可用于测定O2的含量 |
下图各装置中,不能构成原电池的是( )
A、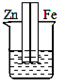 盐酸 |
B、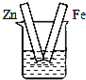 硫酸铜溶液 |
C、 稀硫酸 |
D、 稀硫酸 |
下列过程表达式中,属于电离方程式的是( )
| A、HCO3-+H2O?H2CO3+OH- |
| B、HS-+H2O?S2-+H3O+ |
| C、NH3+H+=NH4+ |
| D、HSO3-+OH-=H2O+SO32- |
镁条和铝片为电极,并用导线连接同时插入NaOH溶液中,下列说法正确的是( )
| A、镁条作负极,电极反应:Mg-2e-=Mg2+ |
| B、铝片作负极,电极反应:Al+4OH--3e--=AlO2-+2H2O |
| C、电流从Al电极沿导线流向Mg电极 |
| D、铝片上有气泡产生 |
 )
)