题目内容
 如图装置是某种气体X的制取装置和收集装置(必要时可加热),所用试剂从下列试剂中选取2~3种,:
如图装置是某种气体X的制取装置和收集装置(必要时可加热),所用试剂从下列试剂中选取2~3种,:硫化亚铁、二氧化锰、铜屑、氯化铵、稀硝酸、浓盐酸、蒸馏水.
请回答下列问题:
(1)气体X的化学式是
(2)所选药品a是
(3)用所选的药品制取X的离子方程式是
(4)在反应刚开始时A中的主要现象是
考点:实验装置综合
专题:实验设计题
分析:(1)制取的气体不需要加热、难溶于水,根据提供的药品可知该气体为NO;
(2)用铜与稀硝酸反应制取一氧化氮气体,a为液体药品、b为固态药品,据此判断药品名称;装置B可以除去二氧化氮气体;
(3)写出铜与稀硝酸反应生成硝酸铜、一氧化氮和水的离子方程式;
(4)根据铜离子的溶液为蓝色溶液、NO与空气中氧气反应生成红棕色的二氧化氮解答.
(2)用铜与稀硝酸反应制取一氧化氮气体,a为液体药品、b为固态药品,据此判断药品名称;装置B可以除去二氧化氮气体;
(3)写出铜与稀硝酸反应生成硝酸铜、一氧化氮和水的离子方程式;
(4)根据铜离子的溶液为蓝色溶液、NO与空气中氧气反应生成红棕色的二氧化氮解答.
解答:
解:(1)在锥形瓶中制取X气体,且不需加热、收集X气体采用排水法(说明X不溶于水),结合给出的试剂可知,制取的气体只能为NO,故答案为:NO;
(2)a中盛放的为液体试剂,应该为稀硝酸;b为固体,应该为铜屑;装置B中盛放是蒸馏水,可以将NO中混有的二氧化氮除去,
故答案为:稀硝酸; 铜屑;蒸馏水洗去NO2;
(3)铜与稀硝酸反应制取NO气体的离子方程式为:3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O,故答案为:3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O;
(4)铜与稀硝酸反应生成硝酸铜、NO气体和水,金属铜溶解,溶液变为蓝色,有气泡产生,瓶内上方出现红棕色气体,
故答案为:铜屑溶解,溶液为浅蓝色,有气泡产生,瓶内上方出现红棕色气体.
(2)a中盛放的为液体试剂,应该为稀硝酸;b为固体,应该为铜屑;装置B中盛放是蒸馏水,可以将NO中混有的二氧化氮除去,
故答案为:稀硝酸; 铜屑;蒸馏水洗去NO2;
(3)铜与稀硝酸反应制取NO气体的离子方程式为:3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O,故答案为:3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O;
(4)铜与稀硝酸反应生成硝酸铜、NO气体和水,金属铜溶解,溶液变为蓝色,有气泡产生,瓶内上方出现红棕色气体,
故答案为:铜屑溶解,溶液为浅蓝色,有气泡产生,瓶内上方出现红棕色气体.
点评:本题考查了铜与稀硝酸反应的实验,题目难度中等,注意掌握常见气体的性质及制备方法,明确化学实验基本操作方法,能够正确书写常见反应的离子方程式、化学方程式,试题培养了学生的分析、理解能力及化学实验能力.

练习册系列答案
相关题目
在石墨的层状晶体里,每一层由无数个正六边形构成,每个碳原子与层内相邻的三个碳原子C-C键结合,等物质的量的石墨与金刚石中C-C键数之比是( )
| A、2:3 | B、2:1 |
| C、3:4 | D、1:1 |
可以用分液漏斗分离的一组混合物是( )
| A、苯和水 | B、酒精和碘 |
| C、醋酸和水 | D、碘和四氯化碳 |
下列有关Ksp说法正确的是( )
| A、某温度下,CaSO4 溶液中C(Ca2+ )?C(SO42-) 就是 Ksp |
| B、25℃时,Fe(OH)3固体在0.01mol/LNH4Cl溶液中的溶解度增大,其Ksp也增大 |
| C、在一定条件下实现 BaSO4+Na2CO3?BaCO3+Na2SO4,说明KSP(BaSO4)>KSP(BaCO3) |
| D、升高温度,若某沉淀溶解平衡逆向移动,Ksp也变小 |
 某芳香化合物H常用作食用香精.用质谱法测得其相对分子质量为162,分子中C、H、O原子个数比为5:5:1.H只有一个支链;它能与溴的四氯化碳溶液发生加成反应.且在碱性条件下能发生水解反应,产物之一是甲醇.G是H的同分异构体.用芳香烃A为原料合成G的路线如图.
某芳香化合物H常用作食用香精.用质谱法测得其相对分子质量为162,分子中C、H、O原子个数比为5:5:1.H只有一个支链;它能与溴的四氯化碳溶液发生加成反应.且在碱性条件下能发生水解反应,产物之一是甲醇.G是H的同分异构体.用芳香烃A为原料合成G的路线如图.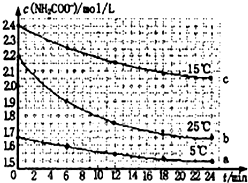 某研究小组在实验室探究氨基甲酸铵(H2NCOONH4)水解反应速率的测定和分解反应平衡常数.
某研究小组在实验室探究氨基甲酸铵(H2NCOONH4)水解反应速率的测定和分解反应平衡常数.