题目内容
 某研究小组在实验室探究氨基甲酸铵(H2NCOONH4)水解反应速率的测定和分解反应平衡常数.
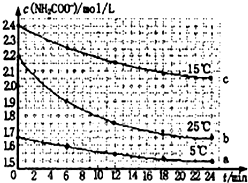
某研究小组在实验室探究氨基甲酸铵(H2NCOONH4)水解反应速率的测定和分解反应平衡常数.(1)已知:H2NCOONH4+2H2O?NH4HCO3+NH3?H2O.该研究小组分别用三份不同初始浓度的氨基甲酸铵溶液测定水解反应速率,得到c(H2NCOO--)随时间变化趋势如图所示.
①25℃时,0~6min氨基甲酸铵水解反应的平均速率为
②对比图中a、b、c哪两条曲线,能得出“水解反应 速率随 温度升高而增大”的结论?
(2)将一定量纯净的氨基甲酸铵置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡:H2NCOONH4(s)?2NH3(g)+CO2(g).实验测得不同温度下的平衡数据列于表:
| 温度(℃) | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 |
| 平衡总压强(kPa) | 5.7 | 8.3 | 12.0 | 17.1 | 24.0 |
| 平衡气体总浓度(×10-3mol/L) | 2.4 | 3.4 | 4.8 | 6.8 | 9.4 |
④氨基甲酸铵分解反应属于
考点:物质的量或浓度随时间的变化曲线,化学平衡的计算
专题:
分析:(1)①根据化学反应速率的公式来计算;
②由图象数据可以得出,用不同初始浓度,不同温度下的平均速率的大小来说明.
(2)③先根据反应 NH2COONH4(s)?2NH3(g)+CO2(g),可知平衡时容器内气体的浓度之比为2:1,由总浓度求出NH3、CO2 的平衡浓度,最后代入平衡常数的表达式来计算;
④根据表中数据判断随着温度升高,平衡移动的方向,从而判断出正反应是吸热还是放热.
②由图象数据可以得出,用不同初始浓度,不同温度下的平均速率的大小来说明.
(2)③先根据反应 NH2COONH4(s)?2NH3(g)+CO2(g),可知平衡时容器内气体的浓度之比为2:1,由总浓度求出NH3、CO2 的平衡浓度,最后代入平衡常数的表达式来计算;
④根据表中数据判断随着温度升高,平衡移动的方向,从而判断出正反应是吸热还是放热.
解答:
解:(1)①化学反应速率V=
=
=0.05mol/(L?min),故答案为:0.05mol/(L?min);
②因25℃反应物起始浓度较小,但0~6min的平均反应速率(曲线的斜率)仍比15℃大,
故答案为:25℃反应物起始浓度较小,但0~6min的平均反应速率(曲线的斜率)仍比15℃大;
(2)③15.0℃时,总浓度为2.4×10-3 mol/L,容器内气体的浓度之比为2:1,故NH3和CO2的浓度分别为1.6×10-3 mol/L、0.8×10-3 mol/L,代入平衡常数表达式:K=(1.6×10-3)2×0.8×10-3 =2.048×10-9,故答案为:2.048×10-9;
④从表中数据可以看出,随着温度升高,气体的总浓度增大,平衡正向移动,则该反应为吸热反应,△H>0,
故答案为:吸热;随着温度升高,平衡气体浓度增大,平衡向正反应方向移动,所以为吸热反应.
| △c |
| △t |
| 2.2mol/L-1.9mol/L |
| 6min |
②因25℃反应物起始浓度较小,但0~6min的平均反应速率(曲线的斜率)仍比15℃大,
故答案为:25℃反应物起始浓度较小,但0~6min的平均反应速率(曲线的斜率)仍比15℃大;
(2)③15.0℃时,总浓度为2.4×10-3 mol/L,容器内气体的浓度之比为2:1,故NH3和CO2的浓度分别为1.6×10-3 mol/L、0.8×10-3 mol/L,代入平衡常数表达式:K=(1.6×10-3)2×0.8×10-3 =2.048×10-9,故答案为:2.048×10-9;
④从表中数据可以看出,随着温度升高,气体的总浓度增大,平衡正向移动,则该反应为吸热反应,△H>0,
故答案为:吸热;随着温度升高,平衡气体浓度增大,平衡向正反应方向移动,所以为吸热反应.
点评:本题是一道考查化学反应速率概念及其计算,化学平衡、化学平衡常数的概念及其计算的试题,要求考生利用图表、进行数据分析判断,吸收、提取有效信息,突出了化学信息运用能力的考查.同时,对于作为化学的基本技能之一的化学计算,渗透在相关的知识块之中,强调计算的实用性以及认识、解决问题的综合性.

练习册系列答案
 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案
相关题目
25℃时水的电离达到平衡:H2O?H++OH-:△H>0下列叙述正确的是( )
| A、向水中加入稀氨水,平衡逆向移动,c(H+)降低 |
| B、向水中加入少量固体醋酸钠,c(H+)增大,Kw不变 |
| C、向水中加入少量固体NH4Cl,平衡逆向移动,c(H+)降低 |
| D、将水加热,Kw增大,pH不变 |
下列说法中,正确的是( )
| A、难溶电解质都是弱电解质 |
| B、难溶电解质在水溶液中达到沉淀溶解平衡时,沉淀和溶解即停止 |
| C、在白色ZnS沉淀上滴加CuSO4溶液,沉淀变黑色,说明CuS比ZnS更难溶于水 |
| D、相同温度下,AgCl在水中的溶解能力与在NaCl溶液中的相同 |
如图装置进行实验,将液体A逐滴加入到固体B中,下列叙述正确的是( )
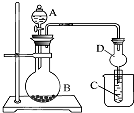

| A、若A为浓盐酸,B为MnO2,C中盛品红溶液,则C中溶液褪色 |
| B、若A为醋酸,B为贝壳,C中盛氯化钙溶液,则C中溶液变浑浊 |
| C、若A为浓氨水,B为生石灰,C中盛AlCl3溶液,则C中先产生白色沉淀后沉淀又溶解 |
| D、实验仪器D可以起到防止溶液倒吸的作用 |
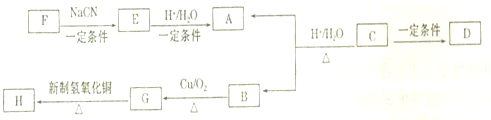
 如图装置是某种气体X的制取装置和收集装置(必要时可加热),所用试剂从下列试剂中选取2~3种,:
如图装置是某种气体X的制取装置和收集装置(必要时可加热),所用试剂从下列试剂中选取2~3种,:


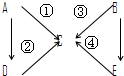 如图表示A-E五种含氮物质相互转化的关系图.其中A、B、C、D常温下都是气体,B为红棕色.
如图表示A-E五种含氮物质相互转化的关系图.其中A、B、C、D常温下都是气体,B为红棕色.