题目内容
几种短周期元素的原子半径及主要化合价如下表:
| 元素代号 | X | Y | Z | W |
| 原子半径/pm | 160 | 143 | 70 | 66 |
| 主要化合价 | +2 | +3 | +3、+5、-3 | -2 |
A.X、Y元素的金属性 X<Y
B.一定条件下,Z单质与W的常见单质直接生成ZW2
C.Y的最高价氧化物对应的水化物能溶于稀氨水
D.一定条件下,W单质可以将Z单质从其氢化物中置换出来
D
解析试题分析:根据元素周期律中化合价与半径的规律判断,Z是N元素,W是O元素,X是Mg,Y是Al元素。A、X、Y元素的金属性X>Y,错误;B、氮气与氧气不能直接反应生成二氧化氮,错误;C、氢氧化铝不溶于氨水,错误;D、在纯氧中氨气与氧气反应生成氮气和水,正确,答案选D。
考点:考查元素的判断及元素周期律的应用,元素化合物的性质

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
能说明M的非金属性比N强的事实是
| A.M的气态氢化物比N的气态氢化物稳定 |
| B.HxM的酸性比HyN的酸性强 |
| C.单质M的熔沸点比单质N的溶沸点高 |
| D.M能将N从它的盐溶液中置换出来 |
短周期元素X、Y、Z的原子序数依次递增,其原子的最外层电子数之和为13,X与Y、Z位于相邻周期,Z原子最外层电子数是X原子内层电子数的3倍或者是Y原子最外层电子数的3倍,下列说法正确的是
| A.X的氢化物溶于水生成弱酸 | B.Z的氢化物的水溶液在空气中存放不易变质 |
| C.Y与X可生成Y3X2型化合物 | D.Z的单质在氧气中燃烧可以生成两种酸性氧化物 |
在元素周期表中,同主族元素的原子具有相同的 ( )
| A.最外层电子数 | B.核电荷数 | C.电子层数 | D.核外电子数 |
我国最新报导的高超导体中,铊(Tl)是其中之一,已知位于第六周期第ⅢA族,关于铊的说法,可能错误的是 ( )
| A.是银白色金属 | B.Tl(OH)3 有两性 |
| C.与稀盐酸反应生成盐酸盐 | D.铊的金属性强于铝的金属性 |
元素周期表中电负性最大的元素是
| A.Fr | B.F | C.H | D.N |
月球上含有丰富的He。关于 He的说法不正确的是
He的说法不正确的是
| A.是一种核素 | B.原子核内有1个中子 |
C.与 He互为同位素 He互为同位素 | D.比 He少一个电子 He少一个电子 |
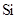
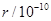 m
m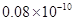 m B.
m B.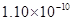 m C.
m C. m D.
m D. m
m