��Ŀ����
��֪��N2��g��+3H2��g��?2NH3��g������H=-Q kJ?mol-1��Q��0�������м���������ͬ���ܱ���������������г���1mol N2��g����3mol H2��g������һ�������´ﵽƽ��ʱ�ų�������ΪQ1 kJ������ͬ���������������г���2mol NH3��g�����ﵽƽ��ʱ���յ�����ΪQ2 kJ����֪Q2=3Q1��������������ȷ���ǣ�������
| A��ƽ��ʱ��������NH3��g��������������������е�С | ||
B��ƽ��ʱ�������������ѹǿΪ��ʼʱѹǿ��
| ||
| C���ﵽƽ��ʱ����������H2��ת����Ϊ25% | ||
D��Q1=
|
���㣺��ѧƽ���Ӱ������,��ѧƽ��ļ���
ר�⣺��ѧƽ��ר��
������A������1molN2��3molH2��ȫ��Ӧ��������2molNH3�����Լ���������ϵ��ƽ��״̬��һ���ģ��Դ˷�����
B������1molN2��3molH2��ȫ��Ӧ��������2molNH3�����Լ���������ϵ��ƽ��״̬��һ���ģ����õ�Чƽ������ƽ��ʱ�����ʵ������ʵ���������ѹǿ֮�ȵ������ʵ���֮�ȷ�����
C�����ݵ�Чƽ��ͷ�Ӧ�ȹ�ϵ�жϣ�N2��H2��ȫ��Ӧʱ����Q����NH3��ȫ�ֽ�ʱ����Ҳ��Q������������е�ת����Ϊx�������Q��x=Q1�������������е�ת����Ϊy����Q��y=Q2 ��Q2=3Q1������Q��y=3Q��x����y=3x���Դ˷�����
D����ӦΪ���淴Ӧ����������ȫ��Ӧ��
B������1molN2��3molH2��ȫ��Ӧ��������2molNH3�����Լ���������ϵ��ƽ��״̬��һ���ģ����õ�Чƽ������ƽ��ʱ�����ʵ������ʵ���������ѹǿ֮�ȵ������ʵ���֮�ȷ�����
C�����ݵ�Чƽ��ͷ�Ӧ�ȹ�ϵ�жϣ�N2��H2��ȫ��Ӧʱ����Q����NH3��ȫ�ֽ�ʱ����Ҳ��Q������������е�ת����Ϊx�������Q��x=Q1�������������е�ת����Ϊy����Q��y=Q2 ��Q2=3Q1������Q��y=3Q��x����y=3x���Դ˷�����
D����ӦΪ���淴Ӧ����������ȫ��Ӧ��
���
�⣺A������1molN2��3molH2��ȫ��Ӧ��������2molNH3�����Լ���������ϵ��ƽ��״̬��һ���ģ�ƽ��ʱ��������NH3��g��������������������е���ȣ���A����
B������1molN2��3molH2��ȫ��Ӧ��������2molNH3�����Լ���������ϵ��ƽ��״̬��һ���ģ������������Ũ����ȫ��ͬ�� N2��H2��ȫ��Ӧʱ����Q����NH3��ȫ�ֽ�ʱ����Ҳ��Q������������е�ת����Ϊx�������Q��x=Q1�������������е�ת����Ϊy����Q��y=Q2 ��Q2=3Q1������Q��y=3Q��x����y=3x������������ϵ��ƽ��״̬��һ���ģ����ԣ�
N2��g��+3H2��g��=2NH3��g��
����ʼ 1 3 0
��ƽ�� 1-x 3-3x 2x
����ʼ 0 0 2
��ƽ�� y 3y 2-2y
����N2�������Դ���1-x=y����x+y=1����������������Ҳһ������y=3x����x=25%��
��ƽ��ʱ����������ʵ���Ϊ1-0.25+3-0.75+0.5=3.5������ѹǿ֮�ȵ������ʵ���֮�ȿ�֪��ƽ��ʱ�������������ѹǿΪ��ʼʱѹǿ��
=
����B����
C����B���֪�ﵽƽ��ʱ����������H2��ת����Ϊ25%����C��ȷ��
D������B���֪��Q��x=Q1����Q1=0.25Q����D����
��ѡC��
B������1molN2��3molH2��ȫ��Ӧ��������2molNH3�����Լ���������ϵ��ƽ��״̬��һ���ģ������������Ũ����ȫ��ͬ�� N2��H2��ȫ��Ӧʱ����Q����NH3��ȫ�ֽ�ʱ����Ҳ��Q������������е�ת����Ϊx�������Q��x=Q1�������������е�ת����Ϊy����Q��y=Q2 ��Q2=3Q1������Q��y=3Q��x����y=3x������������ϵ��ƽ��״̬��һ���ģ����ԣ�
N2��g��+3H2��g��=2NH3��g��
����ʼ 1 3 0
��ƽ�� 1-x 3-3x 2x
����ʼ 0 0 2
��ƽ�� y 3y 2-2y
����N2�������Դ���1-x=y����x+y=1����������������Ҳһ������y=3x����x=25%��
��ƽ��ʱ����������ʵ���Ϊ1-0.25+3-0.75+0.5=3.5������ѹǿ֮�ȵ������ʵ���֮�ȿ�֪��ƽ��ʱ�������������ѹǿΪ��ʼʱѹǿ��
| 3.5 |
| 4 |
| 7 |
| 8 |
C����B���֪�ﵽƽ��ʱ����������H2��ת����Ϊ25%����C��ȷ��
D������B���֪��Q��x=Q1����Q1=0.25Q����D����
��ѡC��
���������⿼�黯ѧƽ��ļ��㣬��Ŀ�Ѷ��еȣ�����ʱע���Чƽ�����������ã�

��ϰ��ϵ�д�
�����Ŀ
����ұ�������Ļ�ѧԭ��������ǣ�������
A��2NaCl�����ڣ�
| ||||
B��MgO+H2
| ||||
C��2Al2O3�����ڣ�
| ||||
D��Fe2O3+3CO
|
������һ�ֻ�ѧ���ʺܻ��õķǽ������ʣ������н�ǿ�������ԣ����������в���ȷ���ǣ�������
| A��ͨ��״���£�����������ܺ�Fe��Ӧ |
| B�����ȵ�ͭ˿�����������ȼ�գ������ػ�ɫ���� |
| C��������H2��Cl2�а�����ȼ�գ�������ɫ���棬����ƿ�ڳ�����״ |
| D����������ˮ��Ӧ����HClO��HCl��������ˮ���ձ�Ϊϡ���� |
���б仯������������ԭ�����͵��ǣ�������
| A����ҵ�����ϳɰ�ʱһ��ѡ����500����¶��½��� |
| B��H2��I2��HI��������ѹ����ɫ���� |
| C���ϳɰ�ʱ����ѭ�������������ԭ�ϵ������� |
| D������ɫ��NO2��ѹ����ɫ�ȱ����ٱ�dz |
�ϳɰ��������������ú��ˮ��ԭ�Ͼ��ಽ��Ӧ�Ƶã����е�һ����ӦΪ��CO��g��+H2O��g��?CO2��g��+H2��g����H��0��Ӧ�ﵽƽ���Ϊ���CO��ת���ʣ����д�ʩ����ȷ���ǣ�������
| A������ѹǿ |
| B�������¶� |
| C������CO��Ũ�� |
| D���������� |
�����������ʼ�ķ�Ӧ����һ�鷴Ӧ�е�ˮ�����������б��ʲ�ͬ���ǣ�������
| A��Cl2+H2O�THCl+HclO |
| B��2F2+2H2O�T4HF+O2 |
| C��3NO2+H2O�T2HNO3+NO |
| D��2Na2O2+2H2O�T4NaOH+O2�� |
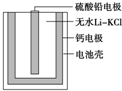 ��ͼΪһ���ȼ����صĻ����ṹ���õ���ܷ�ӦΪPbSO4+2LiCl+Ca�TCaCl2+Li2SO4+Pb����Ϊ����ʵ���ˮLiClKCl������������ں�ؼ���˲��������ܣ������й�˵����ȷ���ǣ�������
��ͼΪһ���ȼ����صĻ����ṹ���õ���ܷ�ӦΪPbSO4+2LiCl+Ca�TCaCl2+Li2SO4+Pb����Ϊ����ʵ���ˮLiClKCl������������ں�ؼ���˲��������ܣ������й�˵����ȷ���ǣ�������| A��������Ӧʽ��Ca+2Cl-+2e-�TCaCl2 |
| B���ŵ�����У�Li+���ƶ� |
| C��ÿת��0.1mol���ӣ�����������20.7gPb |
| D������ʱ��������������ϵ�����������ƣ�ָ�벻ƫת |
�������ӷ���ʽ����д��ȷ���ǣ�������
| A��������Ͷ�뵽ˮ�У�2Na+2H2O=2Na++OH-+H2�� | ||||
B��ʵ������������MnO2+2H++2Cl-
| ||||
| C��ͭ��Ũ���ᷴӦ��Cu+2H+=Cu2++H2�� | ||||
| D��������Ͷ������������Һ�У�2Al+2OH-+2H2O=2AlO2-+3H2�� |