题目内容
100℃时向pH=6的蒸馏水中加入NaHSO4晶体,保持温度不变,测得溶液的pH=2,下列叙述不正确的是( )
| A、此时水的离子积KW=1.0×10-12 |
| B、水电离出的[H+]=1.0×10-10mol/L |
| C、水的电离度随温度升高而升高 |
| D、[H3O+]<[SO42-] |
考点:水的电离
专题:
分析:A、计算出pH=6的蒸馏水中氢离子浓度,根据水的离子积表达式及蒸馏水中c(H+)=c(OH-)计算出水的离子积;
B、硫酸氢钠电离的氢离子抑制了水的电离,溶液中氢氧根离子是水电离的;
C、水的电离是吸热反应,温度升高,水的电离程度增大;
D、根据物水的电离断氢离子与氢氧根离子浓度关系.
B、硫酸氢钠电离的氢离子抑制了水的电离,溶液中氢氧根离子是水电离的;
C、水的电离是吸热反应,温度升高,水的电离程度增大;
D、根据物水的电离断氢离子与氢氧根离子浓度关系.
解答:
解:A、蒸馏水的pH=6,说明c(H+)=c(OH-)=1×10-6mol?L-1,水的离子积Kw=1×10-12,故A正确;
B、水电离出来的氢离子的浓度等于溶液中氢氧根的浓度,c(H+)=c(OH-)=
mol/L=1×10-10mol?L-1,故B正确;
C、由于水的电离过程为吸热反应,升高温度,促进了水的电离,水的电离程度会增大,故C正确;
D、100℃时,蒸馏水中氢离子浓度与氢氧根离子浓度相等,所以呈中性,加入硫酸氢钠溶液呈酸性存在水的电离,氢离子浓度大于硫酸根离子浓度,故D错误;
故选D.
B、水电离出来的氢离子的浓度等于溶液中氢氧根的浓度,c(H+)=c(OH-)=
| 10-12 |
| 0.01 |
C、由于水的电离过程为吸热反应,升高温度,促进了水的电离,水的电离程度会增大,故C正确;
D、100℃时,蒸馏水中氢离子浓度与氢氧根离子浓度相等,所以呈中性,加入硫酸氢钠溶液呈酸性存在水的电离,氢离子浓度大于硫酸根离子浓度,故D错误;
故选D.
点评:本题考查了水的电离,题目难度中等,注意水的离子积常数与溶液的温度有关,明确影响水的电离的因素即可解答,试题基础性强,侧重对学生灵活运用基础知识解决实际问题的能力的培养.

练习册系列答案
 芝麻开花课程新体验系列答案
芝麻开花课程新体验系列答案 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案
相关题目
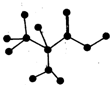 如图是某有机物分子中C、H、O、N四种原子的成键方式示意图(短线表示单键或者双键).下列关于该有机物的说法正确的是.
如图是某有机物分子中C、H、O、N四种原子的成键方式示意图(短线表示单键或者双键).下列关于该有机物的说法正确的是.| A、在一定条件下,可以通过聚合反应生成高分子化合物 |
| B、分子式为C3H6NO2 |
| C、能和NaOH溶液反应,但不能和盐酸溶液反应 |
| D、不能和NaHCO3溶液反应生成CO2 |
化学与生活密切相关,下列说法正确的是( )
| A、油脂和蛋白质都是天然高分子化合物 |
| B、CO2和CH4都是造成温室效应的气体 |
| C、糖类化合物都具有完全相同的官能团 |
| D、磨豆浆的大豆富含蛋白质,豆浆煮沸后蛋白质变成了氨基酸 |
NaNO2是一种食品添加剂,它与酸性KMnO4溶液可发生反应MnO4-+NO2-+X→Mn2++NO3-+H2O(未配平).下列叙述中正确的是( )
| A、生成1molNaNO3需消耗0.4molKMnO4 |
| B、反应过程中溶液的pH减小 |
| C、该反应中NO2-被还原 |
| D、X可以是盐酸 |
关于苯的分子结构和性质的说法中,错误的是( )
| A、苯分子中,有三个碳谈双键,三个碳碳单键,六个碳氢键 |
| B、苯是很好的有机溶剂,它及其同系物常做油漆的溶剂 |
| C、苯易燃,易挥发,所有在储运过程中要注意防火 |
| D、苯在燃烧时,火焰明亮,伴有大量的浓烟,是因为苯分子中碳元素含量较高的缘故 |
下列实验现象描述正确的是( )
| A、氢气在氯气中燃烧生成绿色烟雾 |
| B、碘水中加入少量汽油振荡静置后,下层液体为红色 |
| C、将无色的NO气体与空气混合时,看见气体变为红棕色 |
| D、向FeCl2溶液中滴入KSCN溶液,溶液变为血红色 |