题目内容
16.室内污染的主要成分之一--甲醛(化学式为CH2O),它来源于室内装潢所用的油漆胶合板等材料.下列关于甲醛的说法正确的是( )| A. | 甲醛是一种氧化物 | |
| B. | 甲醛中C、H、O的质量比为6:1:8 | |
| C. | 甲醛分子中含有氢分子 | |
| D. | 甲醛是由一个碳原子和一个水分子构成 |
分析 A、氧化物(oxide)是指由两种元素组成且其中一种是氧元素的化合物,如二氧化碳(CO₂)、氧化钙(CaO)等;
B、甲醛中C、H、O的质量比为12:(1×2):16=6:1:8;
C、分子中不可能还含有其他分子,只可能含有原子;
D、甲醛是由一个碳原子和一个水分子构成,说法错误,理由同C.
解答 解:A、甲醛是由三种元素组成的,所以说一它不是氧化物,说法错误;
B、组成甲醛的各元素的质量比为6:1:8,说法正确;
C、每个甲醛分子由一个碳原子、2个氢原子、1个氧原子构成,说法错误;
D、甲醛分子中不可能还有水分子,说法错误.
故选B.
点评 掌握化学式的书写及意义,学会从组成上识别氧化物的方法,并且要掌握关于化学式计算的方法与技巧.

练习册系列答案
相关题目
6.1mol某金属单质与足量的盐酸反应,放出11.2L H2(标准状况),并转变为与Ne原子电子层结构相同的离子,该金属元素在元素周期表中的位置是( )
| A. | 第三周期第IA族 | B. | 第四周期第IA族 | C. | 第三周期第ⅡA族 | D. | 第四周期第ⅡA族 |
4.常温常压下,将50m13种气态烃的混合物与足量的氧气混合点燃爆炸,恢复到原来状况时,体积共缩小100mL.则3种烃可能是( )
| A. | CH4、C2H4、C3H4 | B. | C2H6、C3H6、C4H6 | C. | CH4、C2H6、C3H8 | D. | C2H4、C2H6、C3H4 |
11.密闭容器中自由移动的活塞两边分别充入空气和H2、O2的混合气体,开始体积比为1:3,若将H2、O2的混合气体点燃引爆,恢复到原来温度(水为液态),活塞右滑停留于容器的正中央,则原来H2、O2的体积比可能为( )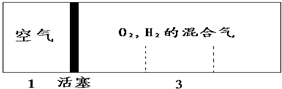
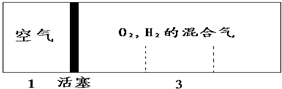
| A. | 2:7 | B. | 5:4 | C. | 1:1 | D. | 7:2 |
1.已知a、b、c、d、e是短周期中原子序数依次增大的5种主族元素,其中元素a、e的单质在常温下呈气态,元素b的原子最外层电子数是其电子层数的2倍,元素c在同周期的主族元素中原子半径最大,元素d的合金是日常生活中常用的金属材料.下列说法正确的是( )
| A. | 原子半径:b<c<d | |
| B. | 金属性:d>c | |
| C. | 化合物ae与ce含有的化学键类型相同 | |
| D. | c、d的最高价氧化物对应的水化物之间能发生反应 |
8.下列物质间的转化在给定条件下能实现的是( )
| A. | Cu$→_{△}^{O_{2}}$CuO$\stackrel{H_{2}O}{→}$Cu(OH)2 | |
| B. | Fe2O3$\stackrel{盐酸}{→}$FeCl3溶液$\stackrel{NaOH、过滤、加热}{→}$Fe2O3 | |
| C. | Mg(OH)2$\stackrel{盐酸}{→}$MgCl2(aq)$\stackrel{电解}{→}$Mg | |
| D. | Na$→_{△}^{O_{2}}$Na2O$\stackrel{CO_{2}}{→}$Na2CO3 |
 .
.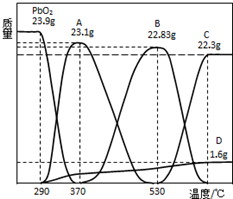 某种铅酸蓄电池具有廉价、长寿命、大容量的特点,它使用的电解质是可溶性的甲基磺酸铅,电池的工作原理:Pb(s)+PbO2(s)+2H2SO4(aq)$?_{充电}^{放电}$2PbSO4(s)+2H2O(l)
某种铅酸蓄电池具有廉价、长寿命、大容量的特点,它使用的电解质是可溶性的甲基磺酸铅,电池的工作原理:Pb(s)+PbO2(s)+2H2SO4(aq)$?_{充电}^{放电}$2PbSO4(s)+2H2O(l)