��Ŀ����
9�� �о��Ϳ���CO2��CO�Ĵ��������ǻ�����������Դ����˫Ӯ�Ŀ��⣮
�о��Ϳ���CO2��CO�Ĵ��������ǻ�����������Դ����˫Ӯ�Ŀ��⣮��1��CO�����ںϳɼ״�����ѹǿΪ0.1MPa�����£������Ϊb L���ܱ������г���a mol CO��2a mol H2���ڴ��������ºϳɼ״���CO��g��+2H2��g��?CH3OH��g��ƽ��ʱCO��ת�������¶ȡ�ѹǿ�Ĺ�ϵ��ͼ��
�������÷�Ӧ���ڷ��ȷ�Ӧ������ȡ����ȡ�����
������100��ʱ����һ�����淴Ӧ��ƽ�ⳣ��Kֵ�ܴԴ˷�Ӧ��˵����ȷ����c������ţ���
a���÷�Ӧʹ�ô������岻��
b���÷�Ӧ�������ں̵ܶ�ʱ�������c���÷�Ӧ�ﵽƽ��ʱ������һ�ַ�Ӧ��ٷֺ�����С
d���÷�Ӧһ���Ƿ��ȷ�Ӧ
���������¶Ⱥ��ݻ����������£�����ƽ����ϵ�г���a mol CO��2a mol H2���ﵽƽ��ʱCO��ת������������������䡱��С������ͬ����ƽ�ⳣ�����䣮
��������ij�¶��£���һ�ݻ�������ܱ������г���2.5mol CO��7.5mol H2����Ӧ����CH3OH��g���ﵽƽ��ʱ��CO��ת����Ϊ90%����ʱ������ѹǿΪ��ʼʱѹǿ��0.55����
��2��ij�¶��£�����CO2��g����H2��g���������1��4��ϣ����ʵ�ѹǿ�ʹ��������¿��Ƶü��飬��֪��
CH4��g��+2O2��g���TCO2��g��+2H2O��l����H=-890.3kJ•mol-1
H2��g��+$\frac{1}{2}$O2��g���TH2O��l����H=-285.8kJ•mol-1
��CO2��g����H2��g����Ӧ���ɼ����Һ̬ˮ���Ȼ�ѧ����ʽΪCO2��g��+4H2��g��=CH4��g��+2H2O��l����H=-252.9kJ•mol-1��
���� ��1����i����ͼ��֪��ѹǿһ��ʱ�����¶����ߣ�CO��ת���ʽ��ͣ��������¶�ƽ�����淴Ӧ�ƶ����ݴ��жϣ�
��ii�����淴Ӧ��ƽ�ⳣ��Խ��˵����Ӧ���еij̶�Խ����˵����Ӧ���ʿ���������˵���÷�Ӧ��ͨ��������һ�����Է���������˵����Ӧ�����Ȼ��Ƿ��ȣ�
��iii�����¶Ⱥ��ݻ����������£�����ƽ����ϵ�г���a mol CO��g����2a mol H2��g������ЧΪ��ԭƽ��Ļ���������һ��ѹǿ��ƽ��������Ӧ�ƶ�����ѧƽ�ⳣ��ֻ���¶�Ӱ�죬��Ũ���أ��¶Ȳ��䣬ƽ�ⳣ�����䣻
��iv������μӷ�Ӧ��CO�����ʵ��������ò���������ƽ��ʱ��Ӧ���������ʵ����仯������������ƽ��ʱ�ܵ����ʵ��������ú��º����£�ѹǿ֮�ȵ������ʵ���֮�Ƚ��
��2�����ݸ�˹������дĿ���Ȼ�ѧ����ʽ��
��� �⣺��1����i����ͼ��֪��ѹǿһ��ʱ�����¶����ߣ�CO��ת���ʽ��ͣ��������¶�ƽ�����淴Ӧ�ƶ���������ӦΪ���ȷ�Ӧ��
�ʴ�Ϊ�����ȣ�
��ii��a�����淴Ӧ��ƽ�ⳣ���ܴ�˵����Ӧ���еij̶Ⱥܴ���˵���÷�Ӧ��ͨ��������һ�����Է������÷�Ӧ������Ҫ�����ſ��Խ��У���a����
b�����淴Ӧ��ƽ�ⳣ���ܴ�˵����Ӧ���еij̶Ⱥܴ���˵���������·�Ӧ���ʺܿ죬��b����
c�����淴Ӧ��ƽ�ⳣ���ܴ�˵����Ӧ���еij̶Ⱥܴ�Ӧ��ƽ��ʱ������һ�ַ�Ӧ��İٷֺ�����С����c��ȷ��
d�����淴Ӧ��ƽ�ⳣ���ܴ�˵����Ӧ���еij̶Ⱥܴ���˵���÷�Ӧ�����Ȼ��Ƿ��ȣ���d����
�ʴ�Ϊ��c��
��iii�����¶Ⱥ��ݻ����������£�����ƽ����ϵ�г���a mol CO��g����2a mol H2��g������ЧΪ��ԭƽ��Ļ���������һ��ѹǿ��ƽ��������Ӧ�ƶ���CO��ת��������ѧƽ�ⳣ��ֻ���¶�Ӱ�죬��Ũ���أ��¶Ȳ��䣬ƽ�ⳣ�����䣬
�ʴ�Ϊ�������䣻
��iv���μӷ�Ӧ��CO�����ʵ���Ϊ2.5mol��90%=2.25mol����
CO��g��+2H2��g��?CH3OH��g�� ���ʵ������١�n
1 2
2.25mol 4.5mol
��ƽ��ʱ�ܵ����ʵ���Ϊ2.5mol+7.5mol-4.5mol=5.5mol�����º�����ѹǿ֮�ȵ������ʵ���֮�ȣ���ƽ��ʱ������ѹǿΪ��ʼʱѹǿ��$\frac{5.5mol}{2.5mol+7.5mol}$=0.55����
�ʴ�Ϊ��0.55��
��2����֪����CH4��g��+2O2��g���TCO2��g��+2H2O��l����H1=-890.3kJ•mol-1
��H2��g��+$\frac{1}{2}$O2��g���TH2O��l����H2=-285.8kJ•mol-1��
���ø�˹���ɣ����ڡ�4-�ٿɵã�CO2��g��+4H2��g��=CH4��g��+2H2O��l����H=4����-285.8kJ•mol-1��-��-890.3kJ•mol-1��=-252.9kJ•mol-1��
�ʴ�Ϊ��CO2��g��+4H2��g��=CH4��g��+2H2O��l����H=-252.9kJ•mol-1��
���� ���⿼�黯ѧƽ��ͼ��ѧƽ���йؼ��㡢��ѧƽ�ⳣ����Ӱ�컯ѧƽ������ء��Ȼ�ѧ����ʽ��д���Ƕ�֪ʶ���ۺ����ã�Ӧ��ǿƽʱ֪ʶ�Ļ��ۣ��Ѷ��еȣ�

| A�� | ���³�ѹ�£�4g H2���еķ�����Ϊ 2NA | |
| B�� | 8g H2O�ڱ�״���µ������22.4L | |
| C�� | 2.3g�����Ʊ�Ϊ������ʱʧȥ�ĵ�����ΪNA | |
| D�� | 17g��������������ĿΪ8NA |
| A�� | ����������Һ������Ͳȡ����ʱ���ӿ̶��� | |
| B�� | ����������Һ����ʱ����������ƿ | |
| C�� | ����4gNaOH����0.20mol/L NaOH��Һ500mLʱ������������� | |
| D�� | ����NaOH��Һʱ����Һδ����ȴ��ע������ƿ���������̶��� |
��1���ٸõ�صĵ缫��Ӧʽ������Ϊ3O2+6H2O-12e-=12OH-������Ϊ2CH4O+16OH--12e-=2CO32-+12H2O��
�����Ըõ��Ϊ��Դ����ʯī���缫���200mL�����������ӵ���Һ��
| ���� | Cu2+ | H+ | Cl- | SO42- |
| c/mol/L | 0.5 | 2 | 2 | 0.5 |
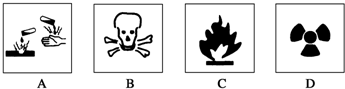
| A�� | Ũ����----Aͼ�� | B�� | �ƾ�----Bͼ�� | ||
| C�� | ����----Cͼ�� | D�� | ��������Ʒ----Dͼ�� |
| A�� | �������Һ���Ǿ�һ���ȶ��ķ�ɢϵ�����ò��ײ������� | |
| B�� | ��������������ֱ���Ͼ�����ͬ������ | |
| C�� | ����ͨ��ʱ��������������ЧӦ����Һ�������ЧӦ | |
| D�� | ��Fe��OH��3��������μ���ϡ�������������� |
| A�� | ����ΪCu������ΪFe���������ҺΪFeCl3��Һ | |
| B�� | ����ΪCu������ΪFe���������ҺΪFe��NO3��2��Һ | |
| C�� | ����ΪFe������ΪCu���������ҺΪFe2��SO4��3��Һ | |
| D�� | ����ΪAg������ΪZn���������ҺΪCuSO4��Һ |