题目内容
某CuSO4、Fe2(SO4)3、H2SO4的混合溶液100mL,已知溶液中阳离子的浓度相等(不考虑水解),且SO42-的物质的量浓度为9mol/L,则此溶液最多溶解Mg的质量为( )
| A、24g | B、18g |
| C、21.6g | D、14.4g |
考点:化学方程式的有关计算
专题:计算题
分析:足量的Mg与CuSO4、Fe2(SO4)3、H2SO4的混合溶液反应最终得到MgSO4,由元素守恒可知,可知n(Mg)=n(MgSO4)=n(SO42-),再根据m=nM计算Mg的质量.
解答:
解:足量的Mg与CuSO4、Fe2(SO4)3、H2SO4的混合溶液反应最终得到MgSO4,由元素守恒可知,可知n(Mg)=n(MgSO4)=n(SO42-)=0.1L×9mol/L=0.9mol,故最多溶解Mg的质量=0.9mol×24g/mol=21.6g,故选C.
点评:本题考查化学方程式有关计算,难度中等,关键是明确足量的Mg与硫酸铁反应得到Fe,注意利用守恒思想解答,简化计算步骤.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列离子方程式正确的是( )
| A、Fe(OH)3溶于氢碘酸:Fe(OH)3+3H+═Fe3++3H2O |
| B、向NaHCO3溶液中加入少量Ca(OH)2溶液:2HCO+Ca2++2OH-═CaCO3↓+CO32-+2H2O |
C、向苯酚溶液中滴加Na2CO3溶液: |
| D、向氯化亚铁溶液中滴加稀硝酸:Fe2++2H++NO═Fe3++NO2↑+H2O |
将2mol SO2和1mol O2充入一容积固定的密闭容器中,在一定条件下发生反应:2SO2(g)+O2(g)?2SO3(g),下列哪些量不再变化时,并不能说明化学反应已达平衡状态( )
| A、混合气体的密度 |
| B、混合气体的压强 |
| C、混合气体的总物质的量 |
| D、混合气体的平均相对分子质量 |
下列说法中正确的是( )
| A、乙烯中碳碳双键的键能是乙烷中碳碳单键的键能的2倍 |
| B、N-O键的极性比C-O键的极性大 |
| C、氮气分子中含有1个σ键和2个π键 |
| D、NH4+中4个N-H键的键能不相同 |
下列离子方程式错误的是( )
| A、小苏打溶液中加入过量的烧碱溶液:HCO3-+OH-=CO32-+H2O |
| B、澄清石灰水中通入过量的CO2:CO2+OH-=HCO3- |
| C、Cl2与水反应生成盐酸和次氯酸Cl2+H2O=2H++Cl-+ClO- |
| D、硫酸与氢氧化钡溶液反应:2H++2OH-+Ba2++SO42-=2H2O+BaSO4↓ |
下列有关实验装置进行的相应实验,能达到实验目的是( )
A、 用如图所示装置进行稀硝酸与铜的反应制取并收集NO |
B、 用如图所示装置进行用已知浓度的氢氧化钠溶液测定盐酸浓度的实验 |
C、 用如图所示装置制取少量Cl2 |
D、 用如图所示装置检验电流的方向 |
有机物H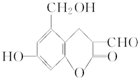 中不含有的官能团是( )
中不含有的官能团是( )
 中不含有的官能团是( )
中不含有的官能团是( )| A、醇羟基 | B、羧基 | C、醛基 | D、酯基 |