题目内容
下列有关实验装置进行的相应实验,能达到实验目的是( )
A、 用如图所示装置进行稀硝酸与铜的反应制取并收集NO |
B、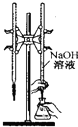 用如图所示装置进行用已知浓度的氢氧化钠溶液测定盐酸浓度的实验 |
C、 用如图所示装置制取少量Cl2 |
D、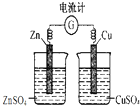 用如图所示装置检验电流的方向 |
考点:化学实验方案的评价
专题:实验评价题
分析:A.稀硝酸和铜反应不需要加热,需要固液混合不加热型装置,NO不溶于水,可以采用排水法收集;
B.酸式滴定管只能盛放酸溶液;
C.稀盐酸和二氧化锰不反应;
D.该装置不能形成闭合回路.
B.酸式滴定管只能盛放酸溶液;
C.稀盐酸和二氧化锰不反应;
D.该装置不能形成闭合回路.
解答:
解:A.硝酸和铜反应制取NO气体,需要固液混合不加热型装置,NO不溶于水,且NO易被氧气氧化生成NO2,所以采用排水法收集NO,故A正确;
B.玻璃中含有二氧化硅,二氧化硅能和氢氧化钠溶液反应生成粘性的硅酸钠而导致活塞打不开,所以酸式滴定管只能盛放酸性溶液,不能盛放碱性溶液,故B错误;
C.加热条件下,用浓盐酸和二氧化锰制取氯气,稀盐酸和二氧化锰不反应,故C错误;
D.该装置不能形成闭合回路,所以不能形成原电池,则没有电流产生,故D错误;
故选A.
B.玻璃中含有二氧化硅,二氧化硅能和氢氧化钠溶液反应生成粘性的硅酸钠而导致活塞打不开,所以酸式滴定管只能盛放酸性溶液,不能盛放碱性溶液,故B错误;
C.加热条件下,用浓盐酸和二氧化锰制取氯气,稀盐酸和二氧化锰不反应,故C错误;
D.该装置不能形成闭合回路,所以不能形成原电池,则没有电流产生,故D错误;
故选A.
点评:本题考查了化学实验方案评价,涉及气体的制取和收集、仪器的使用、原电池原理等知识点,明确实验原理是解本题关键,根据气体的溶解性及密度确定收集方法,注意稀盐酸和二氧化锰不反应,为易错点.

练习册系列答案
 能考试期末冲刺卷系列答案
能考试期末冲刺卷系列答案
相关题目
某CuSO4、Fe2(SO4)3、H2SO4的混合溶液100mL,已知溶液中阳离子的浓度相等(不考虑水解),且SO42-的物质的量浓度为9mol/L,则此溶液最多溶解Mg的质量为( )
| A、24g | B、18g |
| C、21.6g | D、14.4g |
下列说法中正确的是(NA表示阿伏加德罗常数)( )
| A、40g SO2气体所占的体积为11.2L |
| B、7.1g Cl2与水反应转移电子数为0.2NA |
| C、1mol?L-1的CH3COONa溶液中,CH3COO-离子数小于NA |
| D、常温常压下,32g O2和O3的混合气体含氧原子数为2NA |
下列说法正确的是( )
| A、汽车尾气污染物中含有氮的氧化物,是汽油不完全燃烧造成的 |
| B、豆科作物根瘤菌将含氮化合物转化为蛋白质是氮的固定 |
| C、SiO2制成的玻璃纤维,由于导电能力强而被用于制造通讯光缆 |
| D、乙醇、乙烯、乙醛都能使酸性高锰酸钾溶液褪色 |
下列关于电解质溶液的叙述中正确的是( )
| A、Na2CO3、NaHCO3两种盐的溶液中,离子种类不相同 |
| B、常温下1mol?L-1的CH3COOH溶液与1mol?L-1的NaOH溶液等体积混合,所得混合液中[Na+]>[CH3COO-]>[H+]>[OH-] |
| C、物质的量浓度相同的NH4Cl和NH4HSO4两种溶液中,[NH4+]前者小于后者 |
| D、常温下,某溶液中由水电离出的[H+]为1.0×10-5mol?L-1,则此溶液可能是盐酸,也可能是NH4Cl溶液 |
下列叙述正确的是( )
| A、离子晶体中可能含有非极性共价键 |
| B、原子晶体中的相邻原子间只存在非极性共价键 |
| C、分子晶体中一定含有共价键 |
| D、共价化合物中可能含有离子键 |
近日,包括合肥在内的大多城市发生持续雾霾天气,PM2.5数据监测受到了重视.PM2.5是指大气中直径小于2.5微米(1微米=10-6米)的可吸入肺的有害颗粒.下列说法不正确的是( )
| A、PM2.5主要来自工业生产,汽车尾气排放等过程中产生的残留物 |
| B、PM2.5表面积大,能吸附大量有害物质 |
| C、研制开发燃料电池汽车,降低机动车尾气污染,某种程度可以减少PM2.5污染 |
| D、我们要提倡先改善人们的生活质量,随着科技的发展再进行污染的治理 |