题目内容
有下列物质,正盐:钾盐、钠盐、铵盐、钡盐;酸:盐酸、硝酸、醋酸、稀硫酸.在水溶液中符合离子方程式:2H++CO32-═CO2↑+H2O的化学反应的组合共有( )
| A、6个 | B、9个 |
| C、12个 | D、15个 |
考点:离子方程式的书写
专题:离子反应专题
分析:离子方程式表示的是一类反应,如离子方程式2H++CO32-═CO2↑+H2O表示:强酸与可溶性碳酸盐反应生成可溶性盐、水、二氧化碳的反应,据此特点并结合题干中各物质进行解答.
解答:
解:碳酸的钾盐、钠盐、铵盐、钡盐中,BaCO3不溶于水,离子方程式中不能用CO32-表示,其余在溶液中均可用CO32-表示;
四种酸中,醋酸是弱酸,离子方程式中不能用H+表示,
则符合离子方程式2H++CO32-═CO2↑+H2O,存在三种盐(钾盐、钠盐、铵盐)与三种酸(盐酸、硝酸、稀硫酸)可组合出9个反应,且离子方程式相同,
故选B.
四种酸中,醋酸是弱酸,离子方程式中不能用H+表示,
则符合离子方程式2H++CO32-═CO2↑+H2O,存在三种盐(钾盐、钠盐、铵盐)与三种酸(盐酸、硝酸、稀硫酸)可组合出9个反应,且离子方程式相同,
故选B.
点评:本题考查离子反应的书写,为高考常见题型,题目难度中等,注意掌握离子方程式的书写原则,把握离子反应中保留化学式的物质即可解答,试题注重基础知识的考查,培养了学生灵活应用所学知识的能力.

练习册系列答案
相关题目
下列说法正确的是( )
| A、一氧化碳是不稳定的氧化物,它能继续和氧气反应生成稳定的二氧化碳,故反应一定是吸热反应 |
| B、在101kPa时,1mol碳燃烧所放出的热量为碳的燃烧热 |
| C、物质燃烧都需要氧气 |
| D、物质燃烧放出热量的多少与外界条件有关 |
下列关于物质的量的叙述中,正确的是( )
| A、物质的量就是物质的数量 |
| B、1mol任何物质都含有6.02×1023个原子 |
| C、1mol水中含有1mol氢分子和1mol氧原子 |
| D、1mol H2分子中含有2mol H |
以下关于金属的金属性的判断正确的是( )
| A、镁和铝与同浓度的盐酸反应铝没镁反应剧烈,所以铝比镁的金属性强 |
| B、Mg(OH)2溶液的碱性比NaOH溶液的碱性弱,所以镁比钠的金属性强 |
| C、铁能从CuSO4溶液中置换出铜,所以铁比铜的金属性强 |
| D、电解含Ag+和Cu2+的溶液时,Ag+优先放电,所以银比铜的金属性强 |
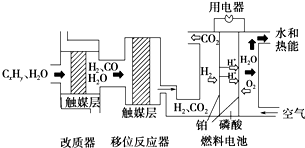 磷酸燃料电池是目前较为成熟的燃料电池之一,其基本组成及反应原理如图所示.下列说法不正确的是( )
磷酸燃料电池是目前较为成熟的燃料电池之一,其基本组成及反应原理如图所示.下列说法不正确的是( )| A、该系统中只存在化学能和电能的相互转化 | ||
B、在移位反应器中,反应CO(g)+H2O(g)
| ||
| C、改质器和移位反应器的作用是将CxHy转化为H2和CO2 | ||
| D、该电池正极的电极反应为O2+4H++4e-=2H2O |
短周期元素W、X、Y、Z的原子序数依次增大,W与Y原子的最外层电子数之和为X原子的最外层电子数的2倍,Z原子的最外层电子数等于其最内层电子数,X、Y、Z的简单离子的电子层结构相同,W的单质是空气中体积分数最大的气体.下列说法正确的是( )
| A、元素Y的气态氢化物比W的稳定 |
| B、元素Y的最高正价与负价绝对值的和等于8 |
| C、化合物XY2与ZY2分子中的化学键类型相同 |
| D、原子半径的大小顺序:r(W)>r(X)>r(Y)>r(Z) |
 X、Y、Z、R、W、M五种元素分别位于周期表中四个紧邻的周期,原子序数依次增大,其它相关信息如下列两表所示:
X、Y、Z、R、W、M五种元素分别位于周期表中四个紧邻的周期,原子序数依次增大,其它相关信息如下列两表所示: