题目内容
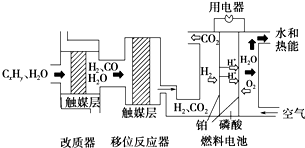 磷酸燃料电池是目前较为成熟的燃料电池之一,其基本组成及反应原理如图所示.下列说法不正确的是( )
磷酸燃料电池是目前较为成熟的燃料电池之一,其基本组成及反应原理如图所示.下列说法不正确的是( )| A、该系统中只存在化学能和电能的相互转化 | ||
B、在移位反应器中,反应CO(g)+H2O(g)
| ||
| C、改质器和移位反应器的作用是将CxHy转化为H2和CO2 | ||
| D、该电池正极的电极反应为O2+4H++4e-=2H2O |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:A、电池中部分化学能转化为热能;
B、根据焓变与温度的关系判断;
C、根据图中改质器和移位反应器里面的产物判断;
D、燃料电池中,正极上得电子发生还原反应,注意结合电解质溶液的酸碱性书写电极反应式.
B、根据焓变与温度的关系判断;
C、根据图中改质器和移位反应器里面的产物判断;
D、燃料电池中,正极上得电子发生还原反应,注意结合电解质溶液的酸碱性书写电极反应式.
解答:
解:A、该系统中存在化学能和电能的相互转化,化学能与热能的转化等,能量转化形式,故A错误;
B、根据移位反应器中CO(g)+H2O(g)═CO2(g)+H2(g)△H<0知,该反应是放热反应,升高温度,导致反应向逆反应方向移动,抑制一氧化碳的转化,故B正确;
C、由图可知通入CxHy,CxHy改质器中转化为H2和CO,CO在移位反应器中转化为CO2,所以改质器和移位反应器的作用是将CxHy转化为H2和CO2,故C正确;
D、燃料电池中,正极上氧化剂得电子和氢离子反应生成水,电极反应式为O2+4H++4e-=2H2O,故D正确.
故选A.
B、根据移位反应器中CO(g)+H2O(g)═CO2(g)+H2(g)△H<0知,该反应是放热反应,升高温度,导致反应向逆反应方向移动,抑制一氧化碳的转化,故B正确;
C、由图可知通入CxHy,CxHy改质器中转化为H2和CO,CO在移位反应器中转化为CO2,所以改质器和移位反应器的作用是将CxHy转化为H2和CO2,故C正确;
D、燃料电池中,正极上氧化剂得电子和氢离子反应生成水,电极反应式为O2+4H++4e-=2H2O,故D正确.
故选A.
点评:本题考查了燃料电池原理,难度不大,注意电极反应式的书写要结合电解质溶液的酸碱性,电解质溶液的酸碱性不同,电极反应式可能不同.

练习册系列答案
 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案
相关题目
下列各元素一定属于主族元素的是( )
| A、X元素的次外层上有18个电子 |
| B、Y元素的最外层上有2个电子 |
| C、Z元素形成的单核阳离子,具有稀有气体元素的核外电子排布 |
| D、R元素形成的单核阴离子,具有稀有气体元素的核外电子排布 |
下列离子方程式书写正确的是( )
| A、NH4HCO3溶液与过量NaOH溶液反应 NH4++OH-═NH3↑+H2O |
| B、过量CO2通入Ca(ClO)2溶液中 ClO-+CO2+H2O═HCO3-+HClO |
| C、向Na2CO3溶液中加入过量CH3COOH溶液 CO32-+2H+═CO2↑+H2O |
| D、向Ba(OH)2溶液中加入少量NaHSO3溶液 2HSO3-+Ba2++2OH-═BaSO3↓+SO32-+2H2O |
下列表示对应化学反应的离子方程式正确的是( )
A、MnO2固体与浓盐酸反应制取Cl2:MnO2+4HCl
| ||||
| B、AlCl3溶液中滴加浓氨水至过量:Al3++4NH3?H2O═AlO2-+4NH4++2H2O | ||||
| C、氯化亚铁溶液中加入硝酸:3Fe2++4H++NO3-═3Fe3++2H2O+NO↑ | ||||
| D、NH4HCO3溶于过量的NaOH溶液中:HCO3-+OH-═CO32-+H2O |
设NA为阿伏加德罗常数的数值,下列叙述正确的是( )
| A、2.24LCO2中含有的原子数为0.3NA |
| B、0.1L3mol?L-1的NH4NO3溶液中含有的NH4+数目为0.3NA |
| C、5.6g铁粉与硝酸反应失去的电子数一定为0.3NA |
| D、4.5gSiO2晶体中含有的硅氧键数目为0.3NA |