题目内容
现有A、B两种链烃饱和一元醇的混合物0.3mol,其质量为13.8g.已知A和B碳原子数均不大于4,且A<B.
(1)混合物中A的分子式为 .
(2)若n(A):n(B)=1:1时,B的结构简式为 .
(3)若n(A):n(B)≠1:1时,B的分子式为 ,n(A):n(B)= .
(1)混合物中A的分子式为
(2)若n(A):n(B)=1:1时,B的结构简式为
(3)若n(A):n(B)≠1:1时,B的分子式为
考点:有机物实验式和分子式的确定
专题:有机物分子组成通式的应用规律
分析:(1)链状饱和一元醇的组成通式为CnH2n+2O,A、B两种链状饱和一元醇的混合物的平均相对分子质量为
=46,乙醇的相对分子质量为46,故一定含有甲醇,A和B碳原子数均不大于4,且A<B,故A为甲醇,则B为C3H8O或C4H10O;
(2)A为甲醇,根据平均相对分子质量,计算B的相对分子质量,再根据组成通式计算B的组成,写出可能结构简式;
(3)A为甲醇,n(A):n(B)≠1:1时,则B的分子式与(2)中B的分子式不同,判断B的结构,设1 mol混合物中CH3OH物质的量为x,则B为(1mol-x),列方程计算x的值,据此计算n(A):n(B).
| 13.8 |
| 0.3 |
(2)A为甲醇,根据平均相对分子质量,计算B的相对分子质量,再根据组成通式计算B的组成,写出可能结构简式;
(3)A为甲醇,n(A):n(B)≠1:1时,则B的分子式与(2)中B的分子式不同,判断B的结构,设1 mol混合物中CH3OH物质的量为x,则B为(1mol-x),列方程计算x的值,据此计算n(A):n(B).
解答:
解:(1)链状饱和一元醇的组成通式为CnH2n+2O,A、B两种链状饱和一元醇的混合物的平均相对分子质量为
=46,
乙醇的相对分子质量为46,故一定含有甲醇,A和B碳原子数均不大于4,且A<B,故A为CH3OH,B为C3H8O或C4H10O,
故答案为:CH4O;
(2)若n(A):n(B)=1:1时,A为CH3OH,令B的相对分子质量为x,则:
=46,解得x=60,
令B为CmH2m+2O,则14m+2+16=60,解得m=3,故B为C3H8O,所以B为1-丙醇或2-丙醇,结构简式为:
CH3CH2CH2OH、CH3CHOHCH3,故答案为:CH3CH2CH2OH、CH3CHOHCH3;
(3)若n(A):n(B)≠1:1时,A为CH3OH,B为C4H10O,
设1 mol混合物中CH3OH物质的量为x,则C4H10O为(1 mol-x),由于CH3OH相对分子质量为32,C4H10O相对分子质量为74,
则:32 g?mol-1?x+74 g?mol-1?(1 mol-x)=46 g,解得x=
mol,所以1 mol-x=
mol,故n(A):n(B)=
mol:
mol=2:1,
故答案为:C4H10O;2:1.
| 13.8 |
| 0.3 |
乙醇的相对分子质量为46,故一定含有甲醇,A和B碳原子数均不大于4,且A<B,故A为CH3OH,B为C3H8O或C4H10O,
故答案为:CH4O;
(2)若n(A):n(B)=1:1时,A为CH3OH,令B的相对分子质量为x,则:
| x+32 |
| 1+1 |
令B为CmH2m+2O,则14m+2+16=60,解得m=3,故B为C3H8O,所以B为1-丙醇或2-丙醇,结构简式为:
CH3CH2CH2OH、CH3CHOHCH3,故答案为:CH3CH2CH2OH、CH3CHOHCH3;
(3)若n(A):n(B)≠1:1时,A为CH3OH,B为C4H10O,
设1 mol混合物中CH3OH物质的量为x,则C4H10O为(1 mol-x),由于CH3OH相对分子质量为32,C4H10O相对分子质量为74,
则:32 g?mol-1?x+74 g?mol-1?(1 mol-x)=46 g,解得x=
| 2 |
| 3 |
| 1 |
| 3 |
| 2 |
| 3 |
| 1 |
| 3 |
故答案为:C4H10O;2:1.
点评:本题考查有机物分子式的确定、有机物的结构与性质等,难度中等,利用平均相对分子质量判断一定含有甲醇是解题关键.

练习册系列答案
 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案
相关题目
在常温下,下列有关溶液中微粒的物质的量浓度关系正确的是( )
| A、.0.1mol?L-1 pH=7.82的NH4HCO3溶液中:c(HCO3-)>c(NH4+)>c(OH-)>c(H+) |
| B、浓度均为0.1mol?L-1的NH3?H2O溶液和NH4Cl溶液等体积混合:[c(NH4+)+c(H+)]>[c(NH3?H2O)+c(OH-)] |
| C、0.1mol?L-1Na2S溶液中:c(OH-)=c(H+)+c(HS-)+c(H2S) |
| D、0.1mol?L-1Na2S溶液与0.1mol?L-1 NaHS溶液等体积混合:2c(Na+)-3c(S2-)=3c(HS-)+3c(H2S) |
下列实验结论或操作、生产方法,准确合理的是( )
| A、某钠盐溶于盐酸产生能使澄清石灰水变浑浊的无色无味气体,说明该钠盐是Na2CO3 |
| B、用饱和Na2CO3溶液除去CO2中混有的HCl |
| C、工业上常采用电解熔融MgO的方法制取金属镁 |
| D、除去MgCl2溶液中少量FeCl3可向其中加入足量Mg(OH)2粉末,充分搅拌后过滤 |
可逆反应H2(g)+I2(g)?2HI,已达平衡的标志是( )
| A、当温度和压强一定时,反应混合气的平均分子量不再改变 |
| B、当温度和压强一定时,混合气体总体积保持不变 |
| C、当温度和压强一定时,反应混合气体的密度不再改变 |
| D、当温度和压强一定时,反应混合气体中各反应物的转化率不再改变 |
将a g甲醛(HCHO)、CH4和CO2的混合气体完全燃烧后,将燃烧后得到的混合气体被足量的Na2O2充分吸收,Na2O2的质量增重了a g,那么CH4与CO2的体积比为( )
| A、1:2 | B、1:1 |
| C、1:3 | D、任意比 |
下列说法不正确的是( )
| A、甲烷和丙烷混合气的密度与同温同压下乙烷的密度相同,混合气中甲烷和丙烷的体积比是1:1 |
| B、A、B两种有机物组成混合物,当混合物质量相等时,无论A、B以何种比例混合,完全燃烧产生CO2的量均相等,符合这一组合的条件A、B两物质可互为同系物 |
| C、等物质的量的烃或烃的含氧衍生物A和B完全燃烧时,消耗氧气的能量相等,则A和B的分子量相差只可能为18n、44n (n为正整数) |
| D、燃烧等质量的烃,耗氧量最多的一定是甲烷 |
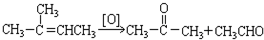
 在上述类似条件下发生反应,请写出反应的方程式:
在上述类似条件下发生反应,请写出反应的方程式: