题目内容
20.下面关于氢化物的叙述正确的是( )| A. | 一个D2O分子所含的中子数为8 | B. | NH3的结构式为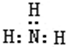 | ||
| C. | HCl的电子式为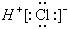 | D. | 热稳定性:H2S<HF |
分析 A.先判断D含有的中子数,再计算D2O分子中含有的中子数;
B.用短线代替所有的共用电子对即为结构式;
C.根据共价化合物电子式的书写规则判断;
D.先判断非金属元素的非金属性,再判断氢化物的稳定性.
解答 解:A.一个重氢原子D含有一个中子,一个氧原子含有8个中子,所以1个D2O分子中所含中子数为10个,故A错误;
B.氨气分子中含有3个N-H键,其结构式为 ,故B正确;
,故B正确;
C、HCl为共价化合物,其电子式为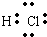 ,故C错误;
,故C错误;
D、由于硫的非金属性比氟弱,所以其氢化物H2S的稳定性比HF弱,故D正确;
故选D.
点评 本题考查了常见化学用语的表示方法,题目难度中等,涉及结构式、原子组成、电子式等知识,明确常见化学用语的书写原则为解答关键,试题培养了学生的规范答题能力.

练习册系列答案
 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案
相关题目
11.已知5KCl+KClO3+3H2SO4═3Cl2+3K2SO4+3H2O,下列说法不正确的是( )
| A. | 氯酸钾是氧化剂 | |
| B. | 被氧化与被还原的氯元素的质量比为5:1 | |
| C. | 3mol氯气生成是有10摩尔电子转移 | |
| D. | 硫酸既不是氧化剂又不是还原剂 |
15.下列比较中,正确的是( )
| A. | 同温度同物质的量浓度时,HF比HCN易电离,NaF溶液的pH比NaCN溶液大 | |
| B. | 0.2 mol•L-1NH4Cl和0.1 mol•L-1 NaOH溶液等体积混合后:c(NH4+)>c(Cl-)>c(Na+)>c(OH-)>c(H+) | |
| C. | 同浓度的下列溶液中,①NH4Al(SO4)2、②NH4Cl、③CH3COONH4、④NH3•H2O;c(NH4+)由大到小的顺序是:①>②>③>④ | |
| D. | 物质的量浓度相等的H2S和NaHS混合溶液中:c(Na+)+c(H+)=c(S2-)+c(HS-)+c(OH-) |
5.下列反应的离子方程式中,错误的是( )
| A. | 铁跟稀硫酸反应 Fe+2H+═Fe2++H2↑ | |
| B. | 碳酸氢钙溶液跟盐酸反应 Ca(HCO3)2+2H+═Ca2++2H2O+2CO2↑ | |
| C. | 醋酸跟氢氧化钾溶液反应 CH3COOH+OH-═CH3COO-+H2O | |
| D. | 碳酸镁跟硫酸反应 MgCO3+2H+═Mg2++H2O+CO2↑ |
10.2012年6月16日我国成功发射神州九号载人宇宙飞船,飞船的太阳能电池板有“飞船血液”之称,它可将太阳能直接转化为电能,我国在砷化镓太阳能电池研究方面国际领先.砷(As)和镓(Ga)都是第四周期元素,分别属于 VA和 IIIA族.下列有关说法正确的是( )
| A. | 由Ga与铝位于同一主族可知Ga既能与盐酸反应又能与氢氧化钠反应 | |
| B. | AsH3的稳定性弱于PH3 | |
| C. | Ga的原子序数比Ca大1 | |
| D. | 太阳能电池属于原电池 |