题目内容
6.实验室可用如下装置(略去部分加持仪器)制取SO2并验收其性质.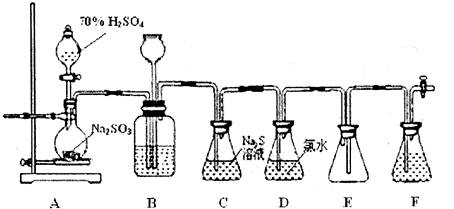
(1)盛放Na2SO3的仪器名称为圆底烧瓶.装置A中发生反应的化学方程式为Na2SO3+H2SO4═Na2SO4+SO2↑+H2O.
(2)仪器组装完成后,关闭两端活塞,向装置B的长颈漏斗内注入液体至形成一段液柱,若一段时间内液柱的高度不变,则整个装置气密性良好.装置B的作用之一是通过观察产生气泡的多少判断SO2生成的快慢,其中的液体最好选择c(填序号).
a.蒸馏水 b.饱和NaOH溶液 c.饱和NaHSO3溶液
(3)装置C中的试剂可以验证二氧化硫的氧化性,相关现象为生成淡黄色沉淀 .
(4)装置D中发生反应的离子方程式为SO2+Cl2+H2O=4H++2Cl-+SO42-.
(5)装置E的作用是防止倒吸.装置F中的试剂为NaOH.
分析 由图可知,A中发生Na2SO3+H2SO4═Na2SO4+SO2↑+H2O,装置B的长颈漏斗内注入液体至形成一段液柱,可检验气密性,C中发生Na2S+H2O+SO2═Na2SO3+H2S、2H2S+SO2═3S↓+2H2O,D中发生SO2+Cl2+H2O=2HCl+H2SO4,E为缓冲装置能防止倒吸,F为尾气处理装置,以此来解答.
解答 解:(1)盛放Na2SO3的仪器名称为圆底烧瓶.装置A中发生反应的化学方程式为Na2SO3+H2SO4═Na2SO4+SO2↑+H2O,
故答案为:圆底烧瓶;Na2SO3+H2SO4═Na2SO4+SO2↑+H2O;
(2)仪器组装完成后,关闭两端活塞,向装置B的长颈漏斗内注入液体至形成一段液柱,若一段时间内液柱的高度不变,则整个装置气密性良好.装置B的作用之一是通过观察产生气泡的多少判断SO2生成的快慢,其中的液体最好选择c,蒸馏水、NaOH溶液都可以吸收二氧化硫,所以不能选取,
故答案为:一段时间内液柱的高度不变;c;
(3)装置C中的试剂可以验证二氧化硫的氧化性,相关现象为生成淡黄色沉淀,故答案为:生成淡黄色沉淀;
(4)D中发生SO2+Cl2+H2O=2HCl+H2SO4,离子反应为SO2+Cl2+H2O=4H++2Cl-+SO42-,故答案为:SO2+Cl2+H2O=4H++2Cl-+SO42-;
(5)缓冲装置能防止倒吸,E装置有缓冲作用而能防止倒吸;SO2有毒且为酸性氧化物,所以不能直接排空,要用碱性溶液吸收,常用NaOH溶液吸收二氧化硫,
故答案为:防止倒吸;NaOH.
点评 本题考查物质的制备实验和性质实验,为高频考点,把握物质的性质、发生的反应、实验装置的作用为解答的关键,侧重分析与实验能力的考查,注意氧化还原反应的应用及尾气处理,题目难度不大.

 课堂练加测系列答案
课堂练加测系列答案 轻松课堂单元测试AB卷系列答案
轻松课堂单元测试AB卷系列答案| A. | Al2O3熔点很高,可用作熔融NaOH的坩埚材料 | |
| B. | 常温下,金属铝不被空气中的氧气氧化,因而能做导线 | |
| C. | 二氧化硅属于硅酸盐材料,玻璃钢属于复合材料 | |
| D. | 生产玻璃和水泥都要用到的原料是石灰石 |
| A. | 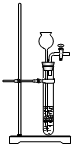 | B. | 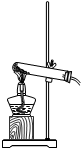 | C. | 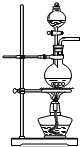 | D. | 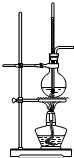 |
| A. | 用湿润的蓝色石蕊试纸检验氨气 | |
| B. | 蒸馏实验中,温度计水银球应位于蒸馏烧瓶支管口处 | |
| C. | 只用BaCl2溶液就可以鉴别SO42-和CO32- | |
| D. | 可用酒精萃取碘水中的碘单质 |
| A. | 最外层一定为8个电子 | |
| B. | 第n层上最多容纳2n2个电子 | |
| C. | M层上的电子一定多于L层上的电子 | |
| D. | 稀有气体元素原子最外层电子数一定是所有元素中最多的 |
| A. | Fe2S3 | B. | Na2S | C. | Cu2S | D. | FeCl3 |