题目内容
一定量的乙醇在氧气不足的情况下燃烧,得到CO、CO2和水的总质量为27.2g,若其中水的质量为10.8g,则CO的质量是( )
| A、2.1g | B、2.6g |
| C、3.8g | D、5.1g |
考点:有关有机物分子式确定的计算
专题:烃及其衍生物的燃烧规律
分析:无论是否完全燃烧,一定质量的C2H5OH燃烧最终得到的水的质量是一定的,也就是1molC2H5OH燃烧得到3molH2O,现在得到10.8gH2O,所以燃烧的C2H5OH一共就是0.2mol,即有n(CO2)+n(CO)=0.4mol,又最后得到混合物质量为27.2g,所以m(CO2)+m(CO)=16.4g,由此分析解答.
解答:
解:无论是否完全燃烧,一定质量的C2H5OH燃烧最终得到的水的质量是一定的,也就是1molC2H5OH燃烧得到3molH2O,现在得到10.8gH2O,所以燃烧的C2H5OH一共就是0.2mol,即有n(CO2)+n(CO)=0.4mol,又最后得到混合物质量为27.2g,所以m(CO2)+m(CO)=16.4g,设CO2 xmol,CO ymol则
解之得:x=0.325,y=0.075,所以CO的质量为0.075×28=2.1g,故选A.
|
解之得:x=0.325,y=0.075,所以CO的质量为0.075×28=2.1g,故选A.
点评:本题考查化学反应方程式的计算,为基础性习题,把握水的质量及CO、CO2的质量、守恒法计算为解答的关键,侧重分析与计算能力的考查,题目难度不大.

练习册系列答案
 53随堂测系列答案
53随堂测系列答案
相关题目
铊是超导材料的组成元素之一,铊在元素周期表中位于第六周期,与铝是同主族元素,元素符号是Tl.以下对铊的单质及其化合物的性质推断不正确的是( )
| A、铊是易导电的银白色金属 |
| B、能生成+3价离子 |
| C、氢氧化铊是两性氢氧化物 |
| D、Tl3+的氧化能力比Al3+强 |
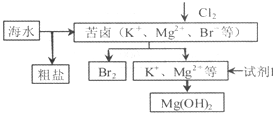 海洋约占地球表面积的71%,对其进行开发利用的部分流程如图所示.下列说法不正确的是( )
海洋约占地球表面积的71%,对其进行开发利用的部分流程如图所示.下列说法不正确的是( )| A、可用BaCl2溶液除去粗盐中的SO42- |
| B、从苦卤中提取Br2的离子方程式为2Br-+Cl2═2C1-十Br2 |
| C、试剂1可以选用Ca(OH)2 |
| D、工业上,电解熔融Mg(OH)2冶炼金属镁 |
对于反应2CO(g)+O2(g)?2CO2(g)(△H<0),在一定条件下建立化学平衡后,下列各条件变化时,能使平衡向正方向移动的是( )
| A、恒容通入少量He |
| B、恒容通入少量CO2 |
| C、升高温度 |
| D、缩小容器体积 |
化学与生产、生活密切相关,下列说法不正确的是( )
| A、Al2O3熔点高,可用于制作耐高温仪器 |
| B、明矾净水与胶体的性质有关 |
| C、H7N9型禽流感病毒在高温条件下被杀死的过程是蛋白质变性 |
| D、高纯度的硅单质用于制作光导纤维,光导纤维有导电性 |
下列鉴别实验中,所选试剂不合理的是( )
| A、用高锰酸钾酸性溶液鉴别甲苯和己烯 |
| B、用水鉴别苯和四氯化碳 |
| C、用饱和碳酸钠溶液鉴别乙酸和乙酸乙酯 |
| D、用新制的氢氧化铜鉴别乙醛和乙醇 |


