题目内容
15.我国“嫦娥Ⅱ号”成功进入月球轨道.据科学家预测,月球的土壤中吸附着数百万吨的${\;}_{2}^{3}$He,每百吨${\;}_{2}^{3}$He核聚变所释放出的能量相当于目前人类一年消耗的能量.在地球上,氦元素主要以${\;}_{2}^{3}$He的形式存在.下列说法正确的是( )
| A. | ${\;}_{2}^{3}$He核聚变是化学变化 | |
| B. | ${\;}_{2}^{3}$He和42He互为同素异形体 | |
| C. | ${\;}_{2}^{3}$He原子核内含仅含有1个中子 | |
| D. | ${\;}_{2}^{4}$He的最外层电子数为2,所以易失电子 |
分析 A.化学变化的实质是旧键的断裂和新建的形成;
B.由同种元素组成的形态不同的单质互为同素异形体;
C.中子数=质量数-质子数;
D.He原子的结构稳定.
解答 解:A.核聚变时原子种类发生变化,不存在旧键的断裂和新键的形成,不属于化学变化,也不属于物理变化,属于核变化,故A错误;
B.32He和42He是原子,不是单质,故B错误;
C.32He原子核内含有2个质子,中子数为3-2=1,故C正确;
D.He原子的结构稳定,既不容易得到电子,也不容易失去电子,故D错误.
故选C.
点评 本题主要考查了原子符号的含义以及同素异形体的概念,难度不大,明确概念是解答本题关键.

练习册系列答案
相关题目
10.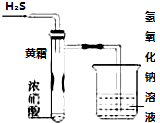 某同学用下列实验装置探究硝酸的性质.根据图示判断下列结论不正确的是
某同学用下列实验装置探究硝酸的性质.根据图示判断下列结论不正确的是
( )
 某同学用下列实验装置探究硝酸的性质.根据图示判断下列结论不正确的是
某同学用下列实验装置探究硝酸的性质.根据图示判断下列结论不正确的是( )
| A. | 试管内壁上“黄霜”的成分是硫 | |
| B. | 该实验探究说明浓硝酸既有氧化性,又有挥发性 | |
| C. | 烧杯内的NaOH溶液的作用是除去尾气,防止尾气污染环境 | |
| D. | H2S用SO2代替,将无明显反应现象 |
20.一定温度时,向2.0L恒容密闭容器中充入2molSO2和1molO2,发生反应:2SO2(g)+O2(g)?2SO3(g).经过一段时间后达到平衡.反应过程中测定的部分数据见下表:
下列说法正确的是( )
| t/s | 0 | t1 | t2 | t3 | t4 |
| n(SO3)/mol | 0 | 0.8 | 1.4 | 1.8 | 1.8 |
| A. | 反应在前t1s的平均速率v(O2)=0.4/t1mol•L-1•s-1 | |
| B. | 保持其他条件不变,体积压缩到1.0L,平衡常数将增大 | |
| C. | 保持温度不变,向该容器中再充入0.3 molSO2、0.1molO2和0.2molSO3,则此时V正>V逆 | |
| D. | 相同温度下,起始时向容器中充入4mol SO3,达到平衡时,SO3的转化率大于10% |
7.下列有机反应属于加聚反应的是( )
| A. | CH4+Cl2$\stackrel{光照}{→}$CH3Cl+HCl | B. |  | ||
| C. |  | D. | 2CH3CH2OH+2Na→2CH3CH2ONa+H2↑ |
4.已知在一定条件下,二个氨基酸分子之间失去一分子水,缩合生成“二肽”.现将甘氨酸[CH2(NH2)-COOH]和丙氨酸[CH3-CH(NH2)-COOH]组成的混合物,在一定条件下发生缩合反应,生成的“二肽”可能有( )
| A. | 1种 | B. | 2种 | C. | 3种 | D. | 4种 |
5.1mol过氧化钠与2mol碳酸氢钠固体混合后,在密闭的容器中加热充分反应,排出气体物质后冷却,残留的固体物质是( )
| A. | Na2CO3、Na2O2 | B. | Na2CO3 | ||
| C. | NaOH、Na2CO3 | D. | Na2O2、NaOH、Na2CO3 |
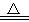 2BCl3+3CO
2BCl3+3CO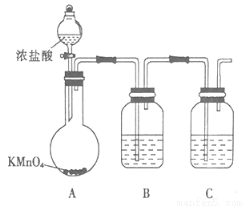

 现有一瓶葡萄糖(C6H12O6)溶液,部分标签如右表所示,请计算(本题只要求写出计算结果):
现有一瓶葡萄糖(C6H12O6)溶液,部分标签如右表所示,请计算(本题只要求写出计算结果):