��Ŀ����
Ԫ�������ڱ��е�λ�ã���ӳ��Ԫ�ص�ԭ�ӽṹ��Ԫ�ص����ʣ���ͼ��Ԫ�����ڱ���һ���֣���1����Ӱ����Ԫ��N��Ԫ�����ڱ��е�λ��Ϊ______��
����Ԫ�������ɣ�����Ԥ�⣺H3AsO4��H3PO4������ǿ����H3AsO4______H3PO4�����á���������������=����ʾ��
��2��Ԫ��S��������ۺ�����۷ֱ�Ϊ______��______����һ�������£�S��H2��Ӧ��һ���ȣ�������Ϊ��Ӧ���еij̶ȣ������ж�����ͬ�����£������ʵ�����S��Se�ֱ��������H2��Ӧ��������̬�⻯������ʵ���______��
��a�� H2S��H2Se ��b�� H2S��H2Se ��c�� H2S=H2Se
��3���ʻ���COS�����ӽṹ�������̼���ӽṹ���ƣ�����ԭ�ӵ�����㶼����8���ӽṹ���õ���ʽ��ʾ�ʻ�����ӵ��γɹ��̣�______��
��4�����ڱ��ϻ��������ͷǽ����ķֽ���______��
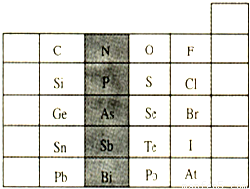
���𰸡���������1��NԪ����2�����Ӳ㣬����������Ϊ5��ͬ���壬���ϵ��·ǽ����Լ���������ۺ����������Խ����
��2��Sλ�ڵڢ�A�壬���Ϊ+6�ۣ���ͼ�Ϊ-2�ۣ�ͬ���壬���ϵ��·ǽ����Լ���������������Խ�ѣ�
��3��COS���ӽṹ�������̼���ӽṹ���ƣ�����ԭ�ӵ�����㶼����8���ӽṹ����C��O��C��S���γ����Թ��е��Ӷԣ�
��4�������ͷǽ����ķֽ�����Si��At֮���б�������ϣ�
����⣺��1��NԪ����2�����Ӳ㣬����������Ϊ5��λ��Ԫ�����ڱ��еڶ����ڵڢ�A�壻ͬ���壬���ϵ��·ǽ����Լ���������ۺ����������Խ�����ǽ�����As��P��������H3AsO4��H3PO4���ʴ�Ϊ���ڶ����ڵ�VA�壻����
��2��Sλ�ڵڢ�A�壬���Ϊ+6�ۣ���ͼ�Ϊ6-8=-2�ۣ�ͬ���壬���ϵ��·ǽ����Լ���������������Խ�ѣ��ɷǽ�����S��Se��֪�������ʵ�����S��Se�ֱ��������H2��Ӧ��������̬�⻯������ʵ���H2S��H2Se���ʴ�Ϊ��+6��-2����b����
��3��COS���ӽṹ�������̼���ӽṹ���ƣ�����ԭ�ӵ�����㶼����8���ӽṹ����C��O��C��S���γ����Թ��е��Ӷԣ��õ���ʽ��ʾ�ʻ�����ӵ��γɹ���Ϊ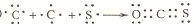 ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
��
��4�������ͷǽ����ķֽ�����Si��At֮���б�������ϣ���ͼ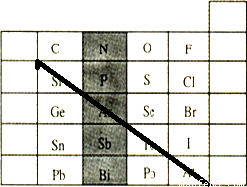 ��
��
�ʴ�Ϊ��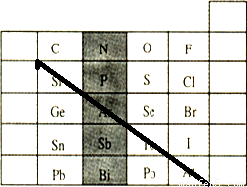 ��
��
���������⿼��λ�á��ṹ�����ʵĹ�ϵ��Ӧ�ã�ע��Ԫ�ص�λ����ṹ�Ķ�Ӧ��ϵ��ͬ�������ʵı仯���ɼ��ɽ����Ŀ�ѶȲ���
��2��Sλ�ڵڢ�A�壬���Ϊ+6�ۣ���ͼ�Ϊ-2�ۣ�ͬ���壬���ϵ��·ǽ����Լ���������������Խ�ѣ�
��3��COS���ӽṹ�������̼���ӽṹ���ƣ�����ԭ�ӵ�����㶼����8���ӽṹ����C��O��C��S���γ����Թ��е��Ӷԣ�
��4�������ͷǽ����ķֽ�����Si��At֮���б�������ϣ�
����⣺��1��NԪ����2�����Ӳ㣬����������Ϊ5��λ��Ԫ�����ڱ��еڶ����ڵڢ�A�壻ͬ���壬���ϵ��·ǽ����Լ���������ۺ����������Խ�����ǽ�����As��P��������H3AsO4��H3PO4���ʴ�Ϊ���ڶ����ڵ�VA�壻����
��2��Sλ�ڵڢ�A�壬���Ϊ+6�ۣ���ͼ�Ϊ6-8=-2�ۣ�ͬ���壬���ϵ��·ǽ����Լ���������������Խ�ѣ��ɷǽ�����S��Se��֪�������ʵ�����S��Se�ֱ��������H2��Ӧ��������̬�⻯������ʵ���H2S��H2Se���ʴ�Ϊ��+6��-2����b����
��3��COS���ӽṹ�������̼���ӽṹ���ƣ�����ԭ�ӵ�����㶼����8���ӽṹ����C��O��C��S���γ����Թ��е��Ӷԣ��õ���ʽ��ʾ�ʻ�����ӵ��γɹ���Ϊ
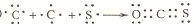 ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
����4�������ͷǽ����ķֽ�����Si��At֮���б�������ϣ���ͼ
 ��
���ʴ�Ϊ��
 ��
�����������⿼��λ�á��ṹ�����ʵĹ�ϵ��Ӧ�ã�ע��Ԫ�ص�λ����ṹ�Ķ�Ӧ��ϵ��ͬ�������ʵı仯���ɼ��ɽ����Ŀ�ѶȲ���

��ϰ��ϵ�д�
�����Ŀ



