题目内容
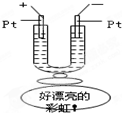 如图所示,在一U型管中装入含有紫色石蕊的Na2SO4试液,通直流电,一段时间后U型管内会形成一个倒立的三色“彩虹”,从右到左颜色的次序是( )
如图所示,在一U型管中装入含有紫色石蕊的Na2SO4试液,通直流电,一段时间后U型管内会形成一个倒立的三色“彩虹”,从右到左颜色的次序是( )| A、蓝、紫、红 |
| B、红、蓝、紫 |
| C、红、紫、蓝 |
| D、紫、红、蓝 |
考点:原电池和电解池的工作原理,电解原理
专题:电化学专题
分析:根据电解原理,电解硫酸钠实质是电解水,阳极产生的是氧气,阴极产生的是氢气,酸遇石蕊显红色,碱遇石蕊显蓝色,酸遇酚酞不变色,碱遇酚酞显红色,据此来回答.
解答:
解:根据电解原理,和电源的正极相连的是阳极,和电源的负极相连的是阴极,电解硫酸钠的实质是电解水,阳极生成氧气,阴极生成氢气,阴极氢离子放电,碱性增强,该极附近呈蓝色,阳极氢氧根离子放电,酸性增强,该极附近呈红色,中间溶液是石蕊的紫色,即从左到右颜色的次序是:红、紫、蓝.
故选C.
故选C.
点评:本题考查学生电解池的工作原理,要求学生熟记教材知识,并会灵活运用.

练习册系列答案
相关题目
下列物质肯定是纯净物的是( )
| A、天然气 |
| B、分子式为C2H6O的物质 |
| C、聚甲基丙烯酸甲酯 |
| D、分子式为C2H5Cl的物质 |
能用来鉴别乙醇、乙酸溶液、葡萄糖溶液、苯四种无色液体的一种试剂是( )
| A、金属钠 |
| B、溴水 |
| C、氢氧化钠溶液 |
| D、新制的Cu(OH)2悬浊液 |
下列有关电化学装置完全正确的是( )
A、 构成铜锌原电池 |
B、 防止Fe被腐蚀 |
C、 铁上镀银 |
D、 铜的精炼 |
在固定体积的密闭容器中进行如下反应:2SO2(g)+O2(g)?2SO3(g).已知反应过程某一时刻SO2、O2、SO3浓度(mol/L)分别为0.2、0.1、0.2,达到平衡时,浓度可能正确的是( )
| A、SO2为0.25mol/L |
| B、SO2,O2分别为0.4,0.2mol/L |
| C、SO2,SO3均为0.15mol/L |
| D、SO3为0.4mol/L |
日常生活中的许多现象与化学反应有关,下列现象与氧化还原反应无关的是( )
| A、大理石雕像被酸雨腐蚀毁坏 |
| B、铜铸塑像上出现铜绿[Cu2(OH)2CO3] |
| C、含亚铁离子的补血药丸采用糖衣包裹 |
| D、充有H2的“喜羊羊”娃娃遇明火发生爆炸 |
HF、H2O、CH4、SiH4四种气态氢化物的热稳定性强弱顺序正确的是( )
| A、CH4<H2O<HF<SiH4 |
| B、SiH4<CH4<H2O<HF |
| C、SiH4<HF<CH4<H2O |
| D、H2O<CH4<HF<SiH4 |
用NA表示阿伏加德罗常数的值,下列说法中正确的是( )
| A、4g重水(D2O)中所含质子数为2NA |
| B、4.48L N2与CO的混合物所含分子数为0.2NA |
| C、12.5mL16 mol?L-1浓硫酸与足量铜反应,转移电子数为0.2NA |
| D、某密闭容器中盛有0.2molSO2和0.1molO2,在一定条件下充分反应,转移电子的数目为0.4NA |
