题目内容
用NA表示阿伏加德罗常数的值,下列说法中正确的是( )
| A、4g重水(D2O)中所含质子数为2NA |
| B、4.48L N2与CO的混合物所含分子数为0.2NA |
| C、12.5mL16 mol?L-1浓硫酸与足量铜反应,转移电子数为0.2NA |
| D、某密闭容器中盛有0.2molSO2和0.1molO2,在一定条件下充分反应,转移电子的数目为0.4NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.重水的摩尔质量为20g/mol,重水中含有10个质子;
B.没有告诉在标准状况下,不能使用标况下的气体摩尔体积计算其物质的量;
C.铜与稀硫酸不反应,铜足量时硫酸不会完全反应,无法计算转移电子数;
D.二氧化硫与氧气的反应为可逆反应,反应物不可能完全转化成生成物.
B.没有告诉在标准状况下,不能使用标况下的气体摩尔体积计算其物质的量;
C.铜与稀硫酸不反应,铜足量时硫酸不会完全反应,无法计算转移电子数;
D.二氧化硫与氧气的反应为可逆反应,反应物不可能完全转化成生成物.
解答:
解:A.4g重水的物质的量为0.2mol,0.2mol重水中含有2mol质子,所含质子数为2NA,故A正确;
B.不是标况下,不能使用标况下的气体摩尔体积计算4.48L混合气体的物质的量,故B错误;
C.12.5mL16 mol?L-1浓硫酸中含有硫酸的物质的量为:16mol/L×0.0125L=0.2mol,铜足量时,随着反应的进行,浓硫酸变成稀硫酸,反应停止,反应生成的二氧化硫小于0.1mol,转移电子小于0.2mol,转移电子数小于0.2NA,故C错误;
D.0.2molSO2和0.1molO2在一定条件下充分反应,该反应为可逆反应,生成的三氧化硫的物质的量小于0.2mol,转移的电子小于0.4mol,转移电子的数目小于0.4NA,故D错误;
故选A.
B.不是标况下,不能使用标况下的气体摩尔体积计算4.48L混合气体的物质的量,故B错误;
C.12.5mL16 mol?L-1浓硫酸中含有硫酸的物质的量为:16mol/L×0.0125L=0.2mol,铜足量时,随着反应的进行,浓硫酸变成稀硫酸,反应停止,反应生成的二氧化硫小于0.1mol,转移电子小于0.2mol,转移电子数小于0.2NA,故C错误;
D.0.2molSO2和0.1molO2在一定条件下充分反应,该反应为可逆反应,生成的三氧化硫的物质的量小于0.2mol,转移的电子小于0.4mol,转移电子的数目小于0.4NA,故D错误;
故选A.
点评:本题考查阿伏加德罗常数的应用,题目难度中等,注意掌握分子、原子、原子核内质子中子及核外电子的构成关系,明确标况下气体摩尔体积的使用条件,选项D为易错点,注意可逆反应特点.

练习册系列答案
 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案 小学学习好帮手系列答案
小学学习好帮手系列答案
相关题目
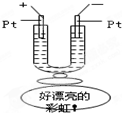 如图所示,在一U型管中装入含有紫色石蕊的Na2SO4试液,通直流电,一段时间后U型管内会形成一个倒立的三色“彩虹”,从右到左颜色的次序是( )
如图所示,在一U型管中装入含有紫色石蕊的Na2SO4试液,通直流电,一段时间后U型管内会形成一个倒立的三色“彩虹”,从右到左颜色的次序是( )| A、蓝、紫、红 |
| B、红、蓝、紫 |
| C、红、紫、蓝 |
| D、紫、红、蓝 |
 甲烷分子中的4个氢原子都可以被取代.若甲烷分子中的4个氢原子都被苯基取代,则可得到的分子如图,对该分子的描述,不正确的是( )
甲烷分子中的4个氢原子都可以被取代.若甲烷分子中的4个氢原子都被苯基取代,则可得到的分子如图,对该分子的描述,不正确的是( )| A、化学式为C25H20 |
| B、所有碳原子都在同一平面上 |
| C、此分子的一氯代物有三种同分异构体 |
| D、此物质属烃类物质 |
下列物质结构与对应的用语表达都正确的是( )
| A、S-C-S:二硫化碳的结构式 |
B、 :苯酚的结构简式 :苯酚的结构简式 |
C、 :氯化铵的电子式 :氯化铵的电子式 |
D、 :钠离子的结构示意图 :钠离子的结构示意图 |
下列说法中,正确的是( )
| A、22 g二氧化碳与标况下11.2 L HCl含有相同的分子数 |
| B、22.4 L N2含阿伏加德罗常数个氮分子 |
| C、在标准状况下,22.4 LSO3的质量为80g |
| D、标准状况下,相同体积的任何气体单质所含的原子数相同 |
下列离子方程式书写正确的是( )
| A、碳酸亚铁溶于稀硝酸:FeCO3+2H+→Fe2++H2O+CO2↑ |
| B、氯化铝溶液中加入过量氢氧化钠溶液:Al3++4OH-=AlO2-+2H2O |
| C、NaHS溶液中加入等物质的量的醋酸:HS-+H+→H2S↑ |
| D、NaHCO3溶液与过量石灰水反应:HCO3-+Ca2++OH-=CaCO3↓+H2O |
下列过程前者属于物理变化,后者属于化学变化的是( )
| A、碳酸钠晶体的风化、硫酸铜检验水 |
| B、煤的干馏、石油的裂化 |
| C、碘的升华、熔融的氯化镁导电 |
| D、煤的气化、用浸泡过高锰酸钾溶液的硅藻土保鲜水果 |
用铂电极电解下列溶液时,阴极和阳极上的主要产物分别为H2和O2的是( )
| A、稀NaOH溶液 |
| B、HCl溶液 |
| C、NaCl溶液 |
| D、酸性AgNO3溶液 |
 一定条件下,在一个3L密闭容器中发生如图反应:
一定条件下,在一个3L密闭容器中发生如图反应: