题目内容
下列有关电化学装置完全正确的是( )
A、 构成铜锌原电池 |
B、 防止Fe被腐蚀 |
C、 铁上镀银 |
D、 铜的精炼 |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:A.含有盐桥的原电池中,电极材料金属与电解质溶液中金属阳离子属于同一种元素;
B.作原电池负极或电解池阳极的金属加速被腐蚀,作原电池正极或电解池阴极的金属被保护;
C.电镀时,镀层作阳极、镀件作阴极;
D.铜的精炼中,粗铜作阳极、纯铜作阴极.
B.作原电池负极或电解池阳极的金属加速被腐蚀,作原电池正极或电解池阴极的金属被保护;
C.电镀时,镀层作阳极、镀件作阴极;
D.铜的精炼中,粗铜作阳极、纯铜作阴极.
解答:
解:A.该装置中金属电极材料与电解质溶液中金属阳离子不属于同一种元素,所以不能构成原电池,故A错误;
B.该装置是电解池,阴极上氢离子放电生成氢气,所以铁作阴极被保护,故B正确;
C.铁上镀银时,镀层银作阳极、镀件Fe作阴极,故C错误;
D.粗铜精炼时,粗铜作阳极、纯铜作阴极,可溶性的硫酸铜作电解质,故D错误;
故选B.
B.该装置是电解池,阴极上氢离子放电生成氢气,所以铁作阴极被保护,故B正确;
C.铁上镀银时,镀层银作阳极、镀件Fe作阴极,故C错误;
D.粗铜精炼时,粗铜作阳极、纯铜作阴极,可溶性的硫酸铜作电解质,故D错误;
故选B.
点评:本题考查原电池及电解池原理,侧重考查学生对基本原理的理解,知道粗铜精炼、电镀时各个电极上发生的反应,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
乙烯和丙烯按1:1(物质的量)聚合时,生成聚合乙丙树脂,该聚合物的结构是( )


| A、① | B、② | C、①④ | D、①② |
可以将反应Zn+Br2=ZnBr2设计成蓄电池,下列4个电极反应①Zn-2e═Zn2+②Zn2++2e═Zn③Br2+2e═2Br- ④2Br--2e═Br2.其中表示充电时的阳极反应和放电时的负极反应分别是( )
| A、②和③ | B、②和① |
| C、③和① | D、④和① |
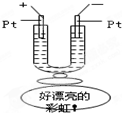 如图所示,在一U型管中装入含有紫色石蕊的Na2SO4试液,通直流电,一段时间后U型管内会形成一个倒立的三色“彩虹”,从右到左颜色的次序是( )
如图所示,在一U型管中装入含有紫色石蕊的Na2SO4试液,通直流电,一段时间后U型管内会形成一个倒立的三色“彩虹”,从右到左颜色的次序是( )| A、蓝、紫、红 |
| B、红、蓝、紫 |
| C、红、紫、蓝 |
| D、紫、红、蓝 |
在2L密闭容器中,发生如下反应:3A(g)+B(g)→C(g)+D(g),若开始时加入的A和B都是4mol,在前10s内A的平均速率为0.12mol/(L?s),则10s时容器内B的物质的量为( )
| A、3.2mol |
| B、2.4mol |
| C、0.8mol |
| D、0.4mol |
下列反应中,属于取代反应的是( )
A、CH2═CH2+H2O
| |||
B、CH4H10
| |||
C、CH3CH3+Br2
| |||
D、2C2H2+5O2
|
下列说法中,正确的是( )
| A、22 g二氧化碳与标况下11.2 L HCl含有相同的分子数 |
| B、22.4 L N2含阿伏加德罗常数个氮分子 |
| C、在标准状况下,22.4 LSO3的质量为80g |
| D、标准状况下,相同体积的任何气体单质所含的原子数相同 |


 元素周期表中第 VIIA族元素的单质及其化合物的用途广泛.
元素周期表中第 VIIA族元素的单质及其化合物的用途广泛.