题目内容
11.填空:(1)下列物质:①O2 ②三氯甲烷 ③CH3CH2CH2OH ④O3 ⑤CHCl3 ⑥CH3OCH2CH3 ⑦612C ⑧CH3CH(OH)CH3 ⑨613C ⑩CH3OH.其中属于同系物的有③⑩或⑧⑩(填序号,下同),互为同分异构体的有③⑥⑧,互为同素异形体的有①④,属于同位素的有⑦⑨.
(2)某些有机物的结构简式可用“键线式”表示,已知某环烷烃是平面结构,它的键线式为“
 ”,其结构如红十字协会的会徽,因此有人将它称为“红十字烷”,写出它的分子式C12H24,当它发生一氯取代物时,能生成2种沸点不同的产物.
”,其结构如红十字协会的会徽,因此有人将它称为“红十字烷”,写出它的分子式C12H24,当它发生一氯取代物时,能生成2种沸点不同的产物.(3)某有机化合物A含碳77.8%,氢为7.40%,其余为氧.A的相对分子质量为甲烷的6.75倍,该有机物的分子式为C7H8O.
分析 (1)结构相似,分子组成相差n个CH2原子团的有机物互为同系物;具有相同分子式、不同结构的有机物互为同分异构体;同种元素的不同单质,互为同素异形体;具有相同质子数、不同中子数的原子为同位素;分子式相同、结构相同的物质为同一种物质;
(2)根据键线式写出分子式;根据分子中的等效氢原子判断一氯代物的种类;
(3)根据相对密度计算有机物的相对分子质量,根据各元素的含量确定有机物中各原子的个数,进而确定有机物分子式.
解答 解:(1)①O2 ②三氯甲烷 ③CH3CH2CH2OH ④O3 ⑤CHCl3 ⑥CH3OCH2CH3 ⑦126C ⑧CH3CH(OH)CH3 ⑨136C ⑩CH3OH
以上组物质中,③CH3CH2CH2OH和⑩CH3OH、⑧CH3CH(OH)CH3和⑩CH3OH的结构相似,分子组成相差n个CH2原子团的有机物,它们互为同系物;
③CH3CH2CH2OH、⑥CH3OCH2CH3、⑧CH3CH(OH)CH3具有相同分子式、不同结构的有机物,二者互为同分异构体;
①O2④O3为同种元素的不同单质,互为同素异形体;
⑦126C 和⑨136C为具有相同质子数、不同中子数的原子,二者为同位素;
故答案为:③⑩或⑧⑩;③⑥⑧;①④;⑦⑨;
(2)由“键线式” 可得分子式为C12H24;该分子是对称的,有2种等效氢原子,一氯化物有2种;
可得分子式为C12H24;该分子是对称的,有2种等效氢原子,一氯化物有2种;
故答案为:C12H24;2;
(3)已知:M(A)=6.75×M(CH4)=16×6.75=108,则有:
N(C)=$\frac{108×77.8%}{12}$=7
N(H)=$\frac{108×7.4%}{1}$=8
N(O)=$\frac{108×(1-77.8%-7.4%)}{16}$=1
所以,A的分子式为C7H8O,
故答案为:C7H8O.
点评 本题考查分子式的书写、同分异构体、同位素等概念的应用、有机物分子式的确定,题目难度不大,注意分子中有几种等效氢原子就有几种一氯代物,侧重于考查学生的分析能力和计算能力.

 寒假创新型自主学习第三学期寒假衔接系列答案
寒假创新型自主学习第三学期寒假衔接系列答案| A. | 乙醇完全燃烧生成CO2和H2O | |
| B. | 0.1 mol乙醇与足量钠反应生成0.05 mol氢气 | |
| C. | 乙醇能溶于水 | |
| D. | 乙醇能脱水 |
| A. | 原子得失电子能力与该原子最外层电子数多少有关 | |
| B. | ⅠA族、ⅡA族元素的阳离子与同周期稀有气体元素的原子具有相同的核外电子排布 | |
| C. | ⅦA族元素的原子随核电荷数的增加,得电子能力逐渐减弱 | |
| D. | 前三周期元素中共有非金属元素12种 |
| A. | 上述过程中,最终被还原的是NO3- | |
| B. | 从上述过程中可以得出结论,氧化性:HNO3>Fe3+>稀H2SO4 | |
| C. | 假设通入的SO2完全反应,则同温同压下,SO2和逸出气体的体积为1:1 | |
| D. | 上述过程中,会产生一种无色的难溶于水的气体 |
| A. | 粗硅制备单晶硅不涉及氧化还原反应 | |
| B. | 硅胶常用做实验时和袋装食品、瓶装药品的干燥剂 | |
| C. | 纯净的硅可做光导纤维的原料 | |
| D. | 水晶项链和餐桌上的瓷盘都是硅酸盐制品 |
 .预测该芳香烃能(填“能”或“不能”)发生该类反应.
.预测该芳香烃能(填“能”或“不能”)发生该类反应.
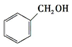 c.
c.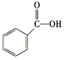
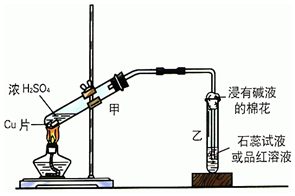 实验室常用如图装置来进行铜跟浓硫酸反应等一系列实验.
实验室常用如图装置来进行铜跟浓硫酸反应等一系列实验.