题目内容
3.已知,过量铁粉与稀硝酸反应的方程式为:3Fe+8HNO3(稀)═3Fe(NO3)2+2NO↑+4H2O,计算:若在标准状况下,当生成2.24L NO气体时,①参加反应的铁质量为多少?
②转移的电子物质的量为多少?
③被还原的氧化剂有多少物质的量?
分析 生成的NO在标准状况时的体积为2.24L,物质的量为n=$\frac{2.24L}{22.4L/mol}$=0.1mol,根据方程式可知,生成2molNO消耗3molFe,并消耗8mol硝酸,但在被消耗的8mol硝酸中,被还原的硝酸为2mol,根据反应后N的化合价为+2价来分析转移的电子的物质的量.
解答 解:①设参加反应的Fe的物质的量为xmol,根据方程式可知,
3Fe+8HNO3(稀)═3Fe(NO3)2+2NO↑+4H2O
3 2
xmol 0.1mol
解得x=0.15mol,则质量m=nM=0.15mol×56g/mol=8.4g.
答:消耗Fe的质量为8.4g;
②由于反应前氮元素为+5价,而反应后N的化合价为+2价,故当生成0.1molNO时转移的电子的物质的量为0.1mol×(5-2)=0.3mol,
答:转移的电子物质的量为0.3mol;
③根据方程式可知,生成2molNO消耗3molFe,并消耗8mol硝酸,但在被消耗的8mol硝酸中,被还原的硝酸为2mol,被还原的硝酸的物质的量等于生成的NO的物质的量,即被还原的硝酸为0.1mol;
答:被还原的氧化剂物质的量为0.1mol.
点评 本题考查了有关方程式的计算、氧化还原反应计算,明确元素的化合价和氧化还原反应的相关概念是解本题的关键,该题解答氧化剂被还原时须注意硝酸中的氮部分被还原,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
13.下列说法中正确的是( )
| A. | SiO2既能溶于NaOH溶液又能溶于氢氟酸,说明SiO2是两性氧化物 | |
| B. | 将Cu片置于浓H2SO4中,无明显现象,说明Cu在冷的浓硫酸中被钝化 | |
| C. | “雷雨发庄稼”的实质是自然固氮 | |
| D. | 自来水厂可用明矾对水进行杀菌消毒 |
14.三氯化硼的熔点为-107℃,沸点为12.5℃,在其分子中键与键之间的夹角为120°,它能水解,有关叙述正确的是( )
| A. | 氯化硼液态时能导电而固态时不导电 | |
| B. | 硼原子以sp3杂化 | |
| C. | 氯化硼分子属极性分子 | |
| D. | 氯化硼遇水蒸气会产生白雾 |
8.下列各组物质中,一定既不是同系物,又不是同分异构体的是( )
| A. | C2H4和C5H6 | B. | 乙醇和二甲醚 | ||
| C. | 正丁烷和异戊烷 | D. | 一溴乙烷和二溴乙烷 |
15.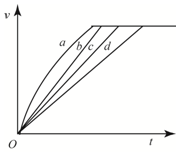 等质量的铁与过量的盐酸在不同的实验条件下进行反应,测得在不同时间(t)内产生气体体积(V)的数据如图所示,根据图示分析实现条件,下列说法中一定不正确的是( )
等质量的铁与过量的盐酸在不同的实验条件下进行反应,测得在不同时间(t)内产生气体体积(V)的数据如图所示,根据图示分析实现条件,下列说法中一定不正确的是( )
 等质量的铁与过量的盐酸在不同的实验条件下进行反应,测得在不同时间(t)内产生气体体积(V)的数据如图所示,根据图示分析实现条件,下列说法中一定不正确的是( )
等质量的铁与过量的盐酸在不同的实验条件下进行反应,测得在不同时间(t)内产生气体体积(V)的数据如图所示,根据图示分析实现条件,下列说法中一定不正确的是( )| 组别 | 对应曲线 | c(HCl)/mol•L-1 | 反应温度/℃ | 铁的状态 |
| 1 | a | 30 | 粉末状 | |
| 2 | b | 30 | 粉末状 | |
| 3 | c | 2.5 | 块状 | |
| 4 | d | 2.5 | 30 | 块状 |
| A. | 第1组实验中盐酸的浓度大于2.5mol•L-1 | |
| B. | 第2组实验中盐酸的浓度大于2.5mol•L-1 | |
| C. | 第3组实验的反应温度低于30℃ | |
| D. | 第4组实验的反应速度最慢 |
12.关于金属元素在自然界存在的情况的叙述中,正确的是( )
| A. | 金属元素仅存在于矿物中 | |
| B. | 金属元素存在于矿物和动物体內,但植物体內不含 | |
| C. | 少数金属元素以游离态存在,大多数金属元素以化合态存在 | |
| D. | 金属元素仅存在矿物中,动物和植物体內也不存在金属元素 |
13.下列有关物质性质的应用错误的是( )
| A. | 硅酸盐可用于制作光导纤维 | |
| B. | FeCl3溶液能与Cu反应,可用于蚀刻印刷电路 | |
| C. | 明矾溶于水后会产生Al(OH)3胶体,可作为净水剂 | |
| D. | 液氨挥发时会吸收大量的热,可作为制冷剂 |
 ”,其结构如红十字协会的会徽,因此有人将它称为“红十字烷”,写出它的分子式C12H24,当它发生一氯取代物时,能生成2种沸点不同的产物.
”,其结构如红十字协会的会徽,因此有人将它称为“红十字烷”,写出它的分子式C12H24,当它发生一氯取代物时,能生成2种沸点不同的产物.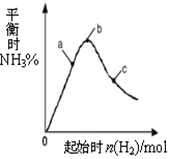 工业上利用N2和H2可以合成NH3,NH3又可以进一步制备联氨(N2H4)等.
工业上利用N2和H2可以合成NH3,NH3又可以进一步制备联氨(N2H4)等.