题目内容
【题目】对于反应![]() ,减小压强,平衡向______(填“正反应”或“逆反应”)方向移动,平衡混合气体的平均相对分子质量在平衡移动时______(填“是”或“否”)发生改变,其原因是____________;下图是反应速率与时间的关系图,
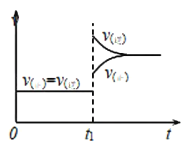
,减小压强,平衡向______(填“正反应”或“逆反应”)方向移动,平衡混合气体的平均相对分子质量在平衡移动时______(填“是”或“否”)发生改变,其原因是____________;下图是反应速率与时间的关系图,![]() 时刻引起正、逆反应速率变化的原因可能是____________(写一条合理原因)。
时刻引起正、逆反应速率变化的原因可能是____________(写一条合理原因)。
【答案】正反应 否 ![]() 和
和![]() 的相对分子质量相同,故它们的平均相对分子质量不变 增大压强或升高温度
的相对分子质量相同,故它们的平均相对分子质量不变 增大压强或升高温度
【解析】
从反应![]() 可以看出,生成物中气体分子数大于反应物中气体分子数,减小压强,平衡向气体分子数增大的方向,即正反应方向移动。由于
可以看出,生成物中气体分子数大于反应物中气体分子数,减小压强,平衡向气体分子数增大的方向,即正反应方向移动。由于![]() 和
和![]() 的相对分子质量相同,故它们的平均相对分子质量不变,即平衡混合气体的平均相对分子质量在平衡移动时不发生改变。从图中可以看出,
的相对分子质量相同,故它们的平均相对分子质量不变,即平衡混合气体的平均相对分子质量在平衡移动时不发生改变。从图中可以看出,![]() 时刻v(逆)>v(正),说明平衡逆向移动;新平衡在原平衡的上方,说明是增大某条件。综合这两点,再结合反应方程式,从浓度、压强、温度三个方面进行分析,可确定改变条件是增大压强或升高温度。
时刻v(逆)>v(正),说明平衡逆向移动;新平衡在原平衡的上方,说明是增大某条件。综合这两点,再结合反应方程式,从浓度、压强、温度三个方面进行分析,可确定改变条件是增大压强或升高温度。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目