��Ŀ����
4�� ij��A���л���ѧ��ҵ�Ļ���ԭ�ϣ������������������һ�����ҵ�ʯ�ͻ�����չˮƽ��A�ɷ�����ͼ��ʾ��һϵ�л�ѧ��Ӧ����ͼ�ش��������⣺
ij��A���л���ѧ��ҵ�Ļ���ԭ�ϣ������������������һ�����ҵ�ʯ�ͻ�����չˮƽ��A�ɷ�����ͼ��ʾ��һϵ�л�ѧ��Ӧ����ͼ�ش��������⣺��1��д��A�ĵ���ʽ
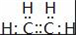 ��D�й����ŵ��������ǻ���
��D�й����ŵ��������ǻ�����2��д��D��CuO��Ӧ�Ļ�ѧ����ʽ��CH3CH2OH+CuO$\stackrel{��}{��}$CH3CHO+Cu+H2O���ں͢�����;���Ʊ�C�����ѡ��;���ڣ�
��3����֪�л���FΪA��һ��ͬϵ���F��A��һ��̼ԭ�ӣ�д��F�����Ӿ۷�Ӧ�Ļ�ѧ����ʽ��nCH2=CHCH3$\stackrel{һ������}{��}$
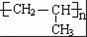 ��
��
���� ��A�IJ���������������һ�����ҵ�ʯ�ͻ�����չˮƽ������һ��ֲ���������ڼ�����AΪCH2�TCH2����ϩ�����������ӳɷ�Ӧ����B��BΪCH3CH3����ϩ��HCl�����ӳɷ�Ӧ����C��CΪCH3CH2Cl����ϩ��ˮ�����ӳɷ�Ӧ����D��DΪCH3CH2OH��CH3CH3����������ȡ����Ӧ����CH3CH2Cl���Դ������
��� �⣺��A�IJ���������������һ�����ҵ�ʯ�ͻ�����չˮƽ������һ��ֲ���������ڼ�����AΪCH2�TCH2����ϩ�����������ӳɷ�Ӧ����B��BΪCH3CH3����ϩ��HCl�����ӳɷ�Ӧ����C��CΪCH3CH2Cl����ϩ��ˮ�����ӳɷ�Ӧ����D��DΪCH3CH2OH��CH3CH3����������ȡ����Ӧ����CH3CH2Cl��
��1��AΪ��ϩ������ʽΪ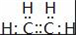 �����еĹ�����Ϊ�ǻ����ʴ�Ϊ��
�����еĹ�����Ϊ�ǻ����ʴ�Ϊ��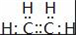 ���ǻ���
���ǻ���
��2��DΪCH3CH2OH��������ͭ�ڼ���������������ȩ������ʽΪ��CΪ�����飬������ϩ���Ȼ��ⷢ���ӳɷ�Ӧ���ɣ������������������ȡ����Ӧ��������ɶ��ָ����
�ʴ�Ϊ��CH3CH2OH+CuO$\stackrel{��}{��}$CH3CHO+Cu+H2O�� �ڣ�
��3����֪�л���FΪA��һ��ͬϵ���F��A��һ��̼ԭ�ӣ�ΪCH2=CHCH3���ɷ����Ӿ۷�Ӧ������ʽΪn CH2=CHCH3$\stackrel{һ������}{��}$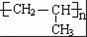 ��
��
�ʴ�Ϊ��n CH2=CHCH3$\stackrel{һ������}{��}$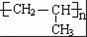 ��
��
���� ����Ϊ�л��ƶ��⣬���ؿ����˳����л���ṹ�����ʣ���Ŀ�Ѷ��еȣ�ע�����ճ����л���ṹ�����ʣ���ȷ�����л���Ӧ�����Ӧ���ͼ��жϷ�������������������ѧ���ķ������������������Ӧ����ѧ֪ʶ���ʵ�������������

| A�� | ����������������Һ��Ӧ�Ʊ�������ϩ��ˮ��Ӧ�Ʊ��� | |
| B�� | �ױ������ƶ������ױ����ױ�������ط�Ӧ�Ʊ����� | |
| C�� | 1-�Ȼ������ƻ���ϩ����ϩ���巴Ӧ��1��2-������� | |
| D�� | ����������ˮ���Ʊ�������Ҵ���������Ҵ����������� |
| ѡ�� | A | B | C | D |
| ʵ�� Ŀ�� | ��ȥKCl������MnO2 | ��10mol•L-1��������100mL 0.1mol•L-1���� | �ú�������NH4Cl���ʵ�NaCl��Һ�Ʊ��Ȼ��ƾ��� | ��ȥ��ϩ������SO2 |
| ʵ��������װ�� | �ձ�������������Һ©�� | 100mL����ƿ�����������ձ� |  |  |
| A�� | A | B�� | B | C�� | C | D�� | D |
| A�� | ��ϩ�������Ҵ�����ʹ��ɫ�����Ը��������Һ��ɫ | |
| B�� | �����Ƶ�������Һ�����ּ�����������ȩ | |
| C�� | ��֬�ڼ�������¿ɷ���ˮ�⣬��ҵ�����ø÷�Ӧ�������� | |
| D�� | ������������֬�����ǡ������ʶ����Է���ˮ�ⷴӦ |

| A�� | ���ڷ����廯���� | B�� | ����ʽΪC27H40O | ||
| C�� | �ܷ����ӳɷ�Ӧ��ȡ����Ӧ | D�� | ����ʹ����KMnO4��Һ��ɫ |
| A�� | CH3OH | B�� |  | C�� |  | D�� |  |

 ��
�� +O2$��_{��}^{Cu}$
+O2$��_{��}^{Cu}$ +2H2O��
+2H2O�� +2nNaOH$��_{��}^{Cu}$n
+2nNaOH$��_{��}^{Cu}$n +n
+n ��+nH2O��
��+nH2O��