��Ŀ����
�밴Ҫ��������и��⣺
��1����������50g�� HCl��NH3��CO2��O2���������У����з�����Ŀ���ٵ��� ��
��2����2.3g ������Ͷ�뵽2.0mol/L 100mL��MgCl2��Һ�У���ȫ��Ӧ��������Һ��Mg2+�����ʵ���Ũ��Ϊ ���ٶ���Ӧ����Һ������䣩��������ơ�þ������Ϊ0.3mol�ֱ���100mLŨ��Ϊ1mol/L��HCl��Һ��Ӧ�����������������Ϊ ��
��3��ij��Һ��ֻ����Na+��Al3+��Cl-��SO
�������ӣ���֪ǰ�������ӵĸ�����Ϊ3��2��1������Һ��Al3+�� SO
�����Ӹ�����Ϊ ��
��4��ʵ����������Ʊ������������������·�Ӧ��2KMnO4+16HCl�T2KCl+2MnCl2+5Cl2��+8H2O
���á�˫���ŷ�����ʾ��������Ӧ����ת�Ƶķ������Ŀ��
�ڸ÷�Ӧ�У��������� ����ԭ������ ���÷�ӦHCl������ ��ѡ���ԭ�ԡ����������ԡ��������ԡ��������ԡ�����
������Ӧת�Ƶĵ�����Ϊ6.02��1023����Ӧ���ɵ�n��Cl2��= ��
��1����������50g�� HCl��NH3��CO2��O2���������У����з�����Ŀ���ٵ���
��2����2.3g ������Ͷ�뵽2.0mol/L 100mL��MgCl2��Һ�У���ȫ��Ӧ��������Һ��Mg2+�����ʵ���Ũ��Ϊ
��3��ij��Һ��ֻ����Na+��Al3+��Cl-��SO
2- 4 |
2- 4 |
��4��ʵ����������Ʊ������������������·�Ӧ��2KMnO4+16HCl�T2KCl+2MnCl2+5Cl2��+8H2O
���á�˫���ŷ�����ʾ��������Ӧ����ת�Ƶķ������Ŀ��
�ڸ÷�Ӧ�У���������
������Ӧת�Ƶĵ�����Ϊ6.02��1023����Ӧ���ɵ�n��Cl2��=
���㣺������ԭ��Ӧ�ļ���,���ʵ�������ؼ���,��ѧ����ʽ���йؼ���
ר�⣺������,������ԭ��Ӧר��
��������1������n=
=
���㣻
��2��n��Na��=
=0.1mol�����Ȼ�þ����Mg2++2OH-=Mg��OH��2������Ϸ�Ӧ�ķ���ʽ���㣻
��3��������Һ�ĵ���غ���㣻
��4����Ӧ2KMnO4+16HCl�T2KCl+2MnCl2+5Cl2��+8H2O�У�MnԪ�ػ��ϼ���+7�۽��͵�+2�ۣ�����ԭ��KMnO4Ϊ��������ClԪ�ػ��ϼ���-1������0�ۣ���������HClΪ��ԭ����
| m |
| M |
| N |
| NA |
��2��n��Na��=
| 2.3g |
| 23g/mol |
��3��������Һ�ĵ���غ���㣻
��4����Ӧ2KMnO4+16HCl�T2KCl+2MnCl2+5Cl2��+8H2O�У�MnԪ�ػ��ϼ���+7�۽��͵�+2�ۣ�����ԭ��KMnO4Ϊ��������ClԪ�ػ��ϼ���-1������0�ۣ���������HClΪ��ԭ����
���
�⣺��1��HCl��NH3��CO2��O2����������CO2����Է������������n=
=
��֪���������Է�������Խ������ʱ��������ʵ���ԽС�����������С����CO2��
�ʴ�Ϊ��CO2��
��2��n��Na��=
=0.1mol����ˮ��Ӧ����NaOH��Ӧ����0.1mol NaOH��n��MgCl2��=0.2mol�����Ȼ�þ����Mg2++2OH-=Mg��OH��2����������0.05mol Mg2+��
��Ӧ��ʣ��n��Mg2+��=0.2mol-0.05mol=0.15mol��c��Mg2+��=
=1.5mol/L��
������ơ�þ������Ϊ0.3mol�ֱ���100mLŨ��Ϊ1mol/L��HCl��Һ��Ӧ����֪þ����������þ���������ᷴӦ��������0.05mol��
���ƿ���ˮ��Ӧ�������������ʵ���Ϊ0.15mol�����������������Ϊ 0.15mol��0.05mol��0.05mol=3��1��1��
�ʴ�Ϊ��1.5 mol/L��3��1��1��
��3����Һ���ڵ���غ㣬Ϊn��Na+��+3n��Al3+��=n��Cl-��+2n��SO42-������֪ǰ�������ӵĸ�����Ϊ3��2��1�������Ϊ3mol��2mol��1mol����n��SO42-��=4mol��
����Һ��Al3+�� SO42-���Ӹ�����Ϊ2��4=1��2��
�ʴ�Ϊ��1��2��
��4���ٷ�Ӧ��KMnO4��MnԪ�ػ��10��������MnCl2��HCl��ClԪ��ʧȥ10����������Cl2����˫���ű�ʾ���÷�Ӧ�ĵ���ת�����Ϊ�� ��
��
�ʴ�Ϊ�� ��
��
��MnԪ����+7�۽��͵�+2�ۣ�ClԪ�صĻ��ϼ���-1�����ߵ�0��������صõ�����������������ԭ����MnCl2��HClʧ�����ǻ�ԭ������Ӧ����KCl���Ȼ��̣����ỹ����Ϊ���ԣ�
�ʴ�Ϊ��KMnO4�� MnCl2����ԭ�ԡ����ԣ�
������Ӧת�Ƶĵ�����Ϊ6.02��1023����1mol���ӣ���Ӧ���ɵ�n��Cl2��=0.5mol��
�ʴ�Ϊ��0.5 mol��
| m |
| M |
| N |
| NA |
�ʴ�Ϊ��CO2��
��2��n��Na��=
| 2.3g |
| 23g/mol |
��Ӧ��ʣ��n��Mg2+��=0.2mol-0.05mol=0.15mol��c��Mg2+��=
| 0.15mol |
| 0.1L |
������ơ�þ������Ϊ0.3mol�ֱ���100mLŨ��Ϊ1mol/L��HCl��Һ��Ӧ����֪þ����������þ���������ᷴӦ��������0.05mol��
���ƿ���ˮ��Ӧ�������������ʵ���Ϊ0.15mol�����������������Ϊ 0.15mol��0.05mol��0.05mol=3��1��1��
�ʴ�Ϊ��1.5 mol/L��3��1��1��
��3����Һ���ڵ���غ㣬Ϊn��Na+��+3n��Al3+��=n��Cl-��+2n��SO42-������֪ǰ�������ӵĸ�����Ϊ3��2��1�������Ϊ3mol��2mol��1mol����n��SO42-��=4mol��
����Һ��Al3+�� SO42-���Ӹ�����Ϊ2��4=1��2��
�ʴ�Ϊ��1��2��
��4���ٷ�Ӧ��KMnO4��MnԪ�ػ��10��������MnCl2��HCl��ClԪ��ʧȥ10����������Cl2����˫���ű�ʾ���÷�Ӧ�ĵ���ת�����Ϊ��
 ��
���ʴ�Ϊ��
 ��
����MnԪ����+7�۽��͵�+2�ۣ�ClԪ�صĻ��ϼ���-1�����ߵ�0��������صõ�����������������ԭ����MnCl2��HClʧ�����ǻ�ԭ������Ӧ����KCl���Ȼ��̣����ỹ����Ϊ���ԣ�
�ʴ�Ϊ��KMnO4�� MnCl2����ԭ�ԡ����ԣ�
������Ӧת�Ƶĵ�����Ϊ6.02��1023����1mol���ӣ���Ӧ���ɵ�n��Cl2��=0.5mol��
�ʴ�Ϊ��0.5 mol��
���������⿼��������ԭ��Ӧ�ļ��㣬�ѶȲ���ע��������ԭ��Ӧ�и��ݻ��ϼ۽��е��йؼ��㣬���յ���ת�Ƶı�ʾ������ע����ؼ��㹫ʽ�����ã�

��ϰ��ϵ�д�
�����Ŀ
��֪����ʱ��0.1mol/LijһԪ��HA��ˮ����0.1%�������룬������������ȷ���ǣ�������
�ٸ���Һ��pH=4��
�������¶ȣ���Һ��pH����
�۴���ĵ���ƽ�ⳣ��ԼΪ1��10-7��
�ܼ�ˮϡ�ͺ����ӵ�Ũ�Ⱦ���С��
����HA�������c��H+��ԼΪˮ�������c��H+����106����
���ʵ�����HA��Ũ�ȣ�HA�ĵ���ƽ�������ƶ�������ƽ�ⳣ������
����������NaOH���壬
����
�ٸ���Һ��pH=4��
�������¶ȣ���Һ��pH����
�۴���ĵ���ƽ�ⳣ��ԼΪ1��10-7��
�ܼ�ˮϡ�ͺ����ӵ�Ũ�Ⱦ���С��
����HA�������c��H+��ԼΪˮ�������c��H+����106����
���ʵ�����HA��Ũ�ȣ�HA�ĵ���ƽ�������ƶ�������ƽ�ⳣ������
����������NaOH���壬
| c(H+) |
| c(HA) |
| A���ڢܢ� | B���٢ۢޢ� |
| C���ڢܢޢ� | D���٢ڢܢݢ� |
���л������ں˴Ź����������ܳ�������壮��������֮��Ϊ3��1���У�������
| A����������� | B�������嶡�� |
| C���Զ��ױ� | D��������� |
 ������ƽ������ƿ���ζ��ܡ���Ͳ����ѧ��ѧ�����ļ�����������֪��Щ������ʹ���Ƕ����о���ѧ�Ļ�����
������ƽ������ƿ���ζ��ܡ���Ͳ����ѧ��ѧ�����ļ�����������֪��Щ������ʹ���Ƕ����о���ѧ�Ļ�����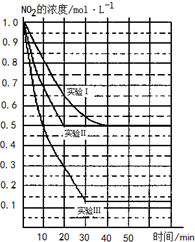 ij�����£���2L�ܱ������з������·�Ӧ��2NO2��g��?2NO��g��+O2��g����H��0�������ֲ�ͬ�����½��У�����NO��O2����ʼŨ�ȶ�Ϊ1.0mol/L��ʵ���Ӧ�¶���ͬ��NO2��Ũ�ȣ�mol?L-1����ʱ�䣨min���ı仯��ͼ��ʾ����ش��������⣺
ij�����£���2L�ܱ������з������·�Ӧ��2NO2��g��?2NO��g��+O2��g����H��0�������ֲ�ͬ�����½��У�����NO��O2����ʼŨ�ȶ�Ϊ1.0mol/L��ʵ���Ӧ�¶���ͬ��NO2��Ũ�ȣ�mol?L-1����ʱ�䣨min���ı仯��ͼ��ʾ����ش��������⣺ ��Դ���������Ϊ��Լ������ᾭ�÷�չ��ƿ����Խ��Խ��Ĺ��ҿ�ʼʵ�С�����ƻ���������̫������Դ��Ѱ�÷�չ���¶�����
��Դ���������Ϊ��Լ������ᾭ�÷�չ��ƿ����Խ��Խ��Ĺ��ҿ�ʼʵ�С�����ƻ���������̫������Դ��Ѱ�÷�չ���¶�����