题目内容
16.下列离子方程式的书写正确的是( )| A. | 铁和稀硫酸反应:2Fe+6H+=2Fe3++3H2↑ | |
| B. | 少量NaHCO3溶液与Ca(OH)2溶液反应:OHˉ+HCO3ˉ+Ca2+=CaCO3↓+H2O | |
| C. | 钠和冷水反应:2Na+2H2O=2 Na++2OHˉ+H2↑ | |
| D. | 过量的CO2和氢氧化钙溶液的反应 OHˉ+CO32-=HCO3ˉ |
分析 A.不符合反应客观事实;
B.碳酸氢钠少量反应生成碳酸钙、氢氧化钠和水;
C.二者反应生成氢氧化钠和氢气;
D.过量二氧化碳与氢氧化钙反应生成碳酸氢钙.
解答 解:A.铁和稀硫酸反应,离子方程式:Fe+2H+=Fe2++H2↑,故A错误;
B.少量NaHCO3溶液与Ca(OH)2溶液反应,离子方程式:OHˉ+HCO3ˉ+Ca2+=CaCO3↓+H2O,故B正确;
C.钠和冷水反应,离子方程式:2Na+2H2O=2 Na++2OHˉ+H2↑,故C正确;
D.过量的CO2和氢氧化钙溶液的反应,离子方程式:OHˉ+CO2=HCO3ˉ,故D错误;
故选:BC.
点评 本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重复分解、氧还原反应及分析与应用能力的考查,题目难度中等,注意反应物用量对反应产物的影响.

练习册系列答案
相关题目
4.2013 年05 月14 日,深圳市人居环境委发布今年首季度的环境状况公报,PM2.5、PM10、二氧化硫、二氧化氮、二氧化碳、臭氧、甲醛等多项空气污染指数比去年同期有所上升,空气质量变差.请回答下列问题:
(1)下列判断正确的是B.
A.CO2为V 形结构分子
B.SO2与O3属于等电子体
C.SO2和SO32-的中心原子均为sp3杂化,其空间构型相同
D.HCHO 分子中只存在σ键不存在π键
(2)空气中的O3含量过高对人体造成伤害,O3常常通过O2放电生成.如表所列数据是在相同条件下,不同物质中氧氧之间的键长和键能的实测数据,其中a和b尚未测出.
①请你根据一个较为可靠的原则可估计出a、b、c、d的大小顺序为d>c>b>a(由大到小),该原则可简述为.
②下列判断正确的是A.
A.O2比O22-稳定
B.O-O 键的键能为494kJ•mol-1
C.O22-离子中存在π键
D.O2转化为O3时只有σ键断裂
(3)氢气作为一种清洁能源,使用氢气可减少SO2的污染,Si60可用作储氢材料,Si60分子中每个硅原子只跟相邻的3个硅原子形成共价键,且每个硅原子最外层都满足8电子稳定结构,则Si60分子中π键的数目为30.
(1)下列判断正确的是B.
A.CO2为V 形结构分子
B.SO2与O3属于等电子体
C.SO2和SO32-的中心原子均为sp3杂化,其空间构型相同
D.HCHO 分子中只存在σ键不存在π键
(2)空气中的O3含量过高对人体造成伤害,O3常常通过O2放电生成.如表所列数据是在相同条件下,不同物质中氧氧之间的键长和键能的实测数据,其中a和b尚未测出.
①请你根据一个较为可靠的原则可估计出a、b、c、d的大小顺序为d>c>b>a(由大到小),该原则可简述为.
| 粒子 | 键长(1.0×10-10m) | 键能(kJ•mol-1) |
| O22- | 1.49 | a |
| O2- | 1.28 | b |
| O2 | 1.21 | c=494 |
| O2+ | 1.12 | d=628 |
A.O2比O22-稳定
B.O-O 键的键能为494kJ•mol-1
C.O22-离子中存在π键
D.O2转化为O3时只有σ键断裂
(3)氢气作为一种清洁能源,使用氢气可减少SO2的污染,Si60可用作储氢材料,Si60分子中每个硅原子只跟相邻的3个硅原子形成共价键,且每个硅原子最外层都满足8电子稳定结构,则Si60分子中π键的数目为30.
1.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 标准状况下22.4LHF中所含电子数为10NA | |
| B. | 100mL12mol•L-1盐酸与足量MnO2共热,转移的电子数为0.6NA | |
| C. | 1mol•L-1 Na2CO3溶液中,CO32-的数目小于NA | |
| D. | 1 mol CH5+中含有的电子数目为10NA |
6.2016年世界环境日中国纪念活动的主题是“改善环境质量,推动绿色发展.”下列说法不符合这一主题的是( )
| A. | 购物时用布袋代替塑料袋 | B. | 农田过量施用农药、化肥 | ||
| C. | 工厂的废水经处理后再排放 | D. | 城市推广使用氢燃料电池客车 |
 如图是一个电化学过程的示意图.
如图是一个电化学过程的示意图.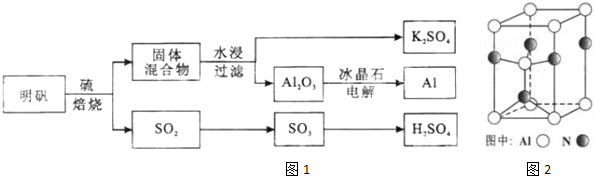
 .
.