题目内容
4.已知在室温的条件下,pH均为5的H2SO4溶液和NH4Cl溶液,回答下列问题:(1)各取5mL上述溶液,分别加热(温度相同),pH较小的是NH4Cl溶液
(2)H2SO4溶液和NH4Cl溶液中由水电离出的c(H+)之比为10-4:1
(3)取5mL NH4Cl溶液,加水稀释至50mL,$\frac{c(N{{H}_{4}}^{+})}{c({H}^{+})}$减小(填“增大”、“减小”或“不变”)
分析 (1)氯化铵水解过程是吸热反应,加热溶液,促进水解氢离子浓度变大,硫酸溶液加热,氢离子浓度基本不变;
(2)依据溶液中离子积常数分析计算;
(3)氯化铵溶液稀释促进水解平衡正向进行,依据溶液中体积相同,离子浓度之比可以比较离子物质的量之比.
解答 解:(1)室温的条件下,pH均为5的H2SO4溶液和NH4Cl溶液,各取5mL上述溶液,分别加热(温度相同),硫酸溶液中氢离子浓度变化不大,氯化铵溶液中水解是系热热反应,加热促进水解,氢离子浓度增大,溶液pH较小的是氯化铵溶液,
故答案为:NH4Cl;
(2)室温的条件下,pH均为5的H2SO4溶液和NH4Cl溶液中存在离子积常数,硫酸溶液中:c(H+)酸×c(OH-)水=10-14,c(OH-)水=10-9mol/L;氯化铵溶液中:c(H+)水×c(OH-)溶液=10-14,水电离的氢离子浓度为:c(H+)水=10-5mol/L,所以H2SO4溶液和NH4Cl溶液中由水电离出的c(H+)之比=$\frac{1{0}^{-9}}{1{0}^{-5}}$=10-4:1,
故答案为:10-4:1;
(3)铵根离子水解平衡NH4++H2O?NH3•H2O+H+,稀释会得到促进,溶液中的铵根离子减小,氢离子增多,$\frac{c(N{{H}_{4}}^{+})}{c({H}^{+})}$ 离子浓度比值减小,
故答案为:减小.
点评 本题考查了盐类水解的应用判断、影响水解平衡的因素分析、溶液中离子积的计算、pH的计算等知识,题目难度中等,理解实质是解题关键,注意熟练掌握溶液酸碱性与溶液pH的关系及计算方法.

练习册系列答案
相关题目
7.下列说法正确的是( )
| A. | 摩尔是表示物质所含质量多少的单位 | |
| B. | 摩尔质量就等于物质式量的6.02×1023倍 | |
| C. | HNO3的摩尔质量是63g | |
| D. | 硫酸和磷酸的摩尔质量相等 |
12.设NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A. | 1 L 0.1 mol/L的氨水中有NA个NH${\;}_{4}^{+}$ | |
| B. | 常温常压下,8 gO2含有4NA个电子 | |
| C. | 标准状况下,22.4 L三氯甲烷含有NA个分子 | |
| D. | 1 mol Na被完全氧化生成Na2O2,失去2NA电子 |
19.设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 标准状况下,11.2 L NO与11.2 L O2混合后所含分子数为0.75NA | |
| B. | pH=13的1.0L Ba(OH)2溶液中含有的OH-数目为0.2NA | |
| C. | 0.1 mol Na2O2晶体中含有0.3NA个离子 | |
| D. | 标准状况下,22.4L甲醇中含有的氧原子数为1.0NA |
9.下列各组粒子在指定溶液中一定能大量共存的一组是( )
| A. | 在KMnO4溶液中:SO42-、Mg2+、CH3CH2OH、NO3- | |
| B. | 在由水电离氢离子浓度为1×10-12mol/L的溶液中:Fe2+、Na+、NO3-、Cl- | |
| C. | 离子浓度相同的溶液中:NH4+、CH3COO-、SO42-、Cu2+ | |
| D. | 无色溶液中:Fe3+、NO3-、Na+、Cl- |
16.构造原理揭示的电子排布能及顺序,实质是各能级能量高低顺序.则下列能级的能量高低顺序正确的是( )
| A. | 5s>4f>4s>3d | B. | 3d>4s>3p>3s | C. | 4s>3s>2s>1s | D. | 5s>4s>4f>3d |
13.向50mL 18mol•L-1H2SO4溶液中加入足量的铜片并加热.充分反应后,被还原的H2SO4的物质的量( )
| A. | 小于0.45 mol | B. | 等于0.45 mol | ||
| C. | 在0.45 mol和0.90 mol之间 | D. | 大于0.90 mol |
14.下列实验装置或操作能达到实验目的是( )
| A. |  定量测定反应速率 | B. | 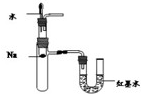 验证Na和水反应的热效应 | ||
| C. |  酸碱中和滴定 | D. |  证明氧化性Cl2>Br2>I2 |
