题目内容
12.设NA为阿伏加德罗常数的数值,下列说法正确的是( )| A. | 1 L 0.1 mol/L的氨水中有NA个NH${\;}_{4}^{+}$ | |
| B. | 常温常压下,8 gO2含有4NA个电子 | |
| C. | 标准状况下,22.4 L三氯甲烷含有NA个分子 | |
| D. | 1 mol Na被完全氧化生成Na2O2,失去2NA电子 |
分析 A、一水合氨是弱电解质,电离是微弱的;
B、氧气由氧原子构成;
C、标况下,三氯甲烷为液态;
D、根据反应后钠变为+1价来分析.
解答 解:A、一水合氨是弱电解质,电离是微弱的,1L0.1mol•L-1的氨水中有NH4+数目小于NA个,故A错误;
B、氧气由氧原子构成,8g氧气中含有的氧原子的物质的量n=$\frac{8g}{16g/mol}$=0.5mol,而氧原子中含8个电子,故0.5mol氧原子中含4mol电子即4NA个,故B正确;
C、标况下,三氯甲烷为液态,不能根据气体摩尔体积来计算其物质的量,故C错误;
D、反应后钠变为+1价,故1mol钠失去1mol电子即NA个,故D错误.
故选B.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 智慧课堂密卷100分单元过关检测系列答案
智慧课堂密卷100分单元过关检测系列答案 单元期中期末卷系列答案
单元期中期末卷系列答案
相关题目
15.下列各种情况下,常温下溶液中一定能大量存在的离子组是( )
| A. | 由水电离出的c(H+)=l×10-12mol/L的溶液中:K+、Ba2+、Cl-、NO3- | |
| B. | 无色溶液中可能大量存在:Al3+、NH4+、Cl-、S2- | |
| C. | pH=7的中性溶液中:Fe3+、K+、Cl-、SO42- | |
| D. | 酸性溶液中可能大量存在:Na+、ClO-、SO42-、CN- |
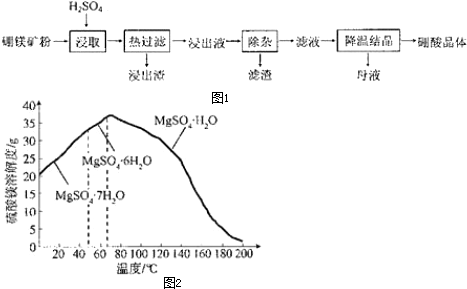
3.硼酸(H3BO3)大量应用于玻璃制造行业,以硼镁矿(2MgO.B2O3.H2O、SiO2及少量Fe3O4、CaCO3、Al2O3 )为原料生产硼酸的工艺流程如图1:
表一:硼酸在不同温度下的溶解度(s)
表二:金属阳离子以氢氧化物形式完全沉淀时(c≤1.0×10-5mol•L-1)的pH
(1)写出2MgO•B2O3•H2O浸取生成H3BO3的化学方程式:2MgO•B2O3•H2O+2H2SO4=2MgSO4+2H3BO3;
(2)除杂操作过程中加入MgO调节溶液pH的目的除去溶液中的Al3+、Fe3+杂质;
(3)“浸取”后,采用“热过滤”的目的是防止温度下降时H3BO3从溶液中析出,浸出渣的成分SiO2、CaSO4;
(4)根据题中所给条件计算Fe(OH)3的Kap值1×10-38;
(5)“母液”可用于回收硫酸镁,已知硫酸镁的溶解度随温度变化的曲线如图2所示,且溶液的沸点随压强增大而升高.为了从“母液”中充分回收 MgSO4.H2O,应采取的操作是a.
a.加压升温结晶b.降温结晶c.蒸发结晶.

表一:硼酸在不同温度下的溶解度(s)
| 温度 | 20℃ | 40℃ | 60℃ | 100℃ |
| 溶解度(s) | 5.0g | 8.7g | 14.8g | 40.2g |
| 金属阳离子 | Fe3+ | Al3+ | Fe2+ | Mg2+ |
| pH | 3.0 | 5.2 | 9.7 | 12.4 |
(2)除杂操作过程中加入MgO调节溶液pH的目的除去溶液中的Al3+、Fe3+杂质;
(3)“浸取”后,采用“热过滤”的目的是防止温度下降时H3BO3从溶液中析出,浸出渣的成分SiO2、CaSO4;
(4)根据题中所给条件计算Fe(OH)3的Kap值1×10-38;
(5)“母液”可用于回收硫酸镁,已知硫酸镁的溶解度随温度变化的曲线如图2所示,且溶液的沸点随压强增大而升高.为了从“母液”中充分回收 MgSO4.H2O,应采取的操作是a.
a.加压升温结晶b.降温结晶c.蒸发结晶.
17.下列物质既能与盐酸反应,又能与氢氧化钠溶液反应的是( )
①Ca(OH)2②Al2O3③Ca(HCO3)2④Al(OH)⑤NaHSO4⑥Al⑦(NH4)2S.
①Ca(OH)2②Al2O3③Ca(HCO3)2④Al(OH)⑤NaHSO4⑥Al⑦(NH4)2S.
| A. | ②④⑥ | B. | ②③⑤⑥ | C. | ①③④⑥ | D. | ②③④⑥⑦ |
1.某一周期的第ⅡA族元素的原子序数为Z,那么同一周期的第ⅢA族元素的原子序数( )
| A. | 可能是Z+1或Z+11或Z+25 | B. | 只有Z+1 | ||
| C. | 可能是Z+1或Z+11 | D. | 可能是Z+2或Z+8或Z+18 |
2.下列化学用语能正确表示相应意义的是( )
| A. | 乙烯的结构简式CH2CH2 | B. | 丁烷的结构简式CH3(CH2)2CH3 | ||
| C. | 四氯化碳的电子式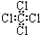 | D. | 苯的分子式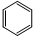 |
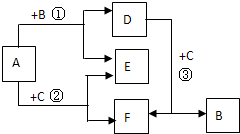 A~F都是中学化学常见物质,它们间的相互转化关系如图所示,其中A、D、F是化合物,E是非金属单质.
A~F都是中学化学常见物质,它们间的相互转化关系如图所示,其中A、D、F是化合物,E是非金属单质.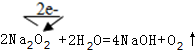 .
.