题目内容
14.下列实验装置或操作能达到实验目的是( )| A. |  定量测定反应速率 | B. | 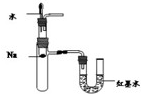 验证Na和水反应的热效应 | ||
| C. | 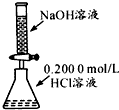 酸碱中和滴定 | D. | 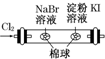 证明氧化性Cl2>Br2>I2 |
分析 A.过氧化氢与二氧化锰反应生成氧气,氧气可能从长颈漏斗逸出;
B.Na和水反应放热,U型管内左侧液面下降;
C.酸式滴定管不能盛放NaOH溶液;
D.氯气与NaBr、KI均反应.
解答 解:A.过氧化氢与二氧化锰反应生成氧气,氧气可能从长颈漏斗逸出,不能测定反应速率,可将长颈漏斗改为分液漏斗,故A错误;
B.Na和水反应放热,U型管内左侧液面下降,则该实验可验证Na和水反应的热效应,故B正确;
C.酸式滴定管不能盛放NaOH溶液,不能进行中和滴定实验,故C错误;
D.氯气与NaBr、KI均反应,则该实验不能验证溴、碘的氧化性,故D错误;
故选B.
点评 本题考查化学实验方案的评价,为高频考点,涉及反应速率测定、反应热效应、中和滴定及氧化性比较等,把握反应原理及实验装置的作用为解答的关键,侧重分析与实验能力的考查,题目难度不大.

练习册系列答案
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案
相关题目
5.下列区别物质的方法错误的是( )
| A. | 铝与铝合金-比较硬度 | B. | 用水区别氯化钠和硝酸铵固体 | ||
| C. | 用燃烧的方法区别羊毛和涤纶 | D. | 用燃着的木条鉴别氮气与二氧化碳 |
2.下列化学用语能正确表示相应意义的是( )
| A. | 乙烯的结构简式CH2CH2 | B. | 丁烷的结构简式CH3(CH2)2CH3 | ||
| C. | 四氯化碳的电子式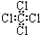 | D. | 苯的分子式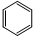 |
9.下列实验叙述有错误的是( )
| A. | 实验室制取乙烯气体时,将温度计的水银球放入液面以下 | |
| B. | 向淀粉水解后的溶液中加入碘水,溶液变蓝,证明淀粉尚未水解 | |
| C. | 证明分子CH2=CH-CHO既含有醛基又含有C=C,可先向溶液中先加入足量的银氨溶液加热,充分反应后,再加入足量的溴水 | |
| D. | 在蔗糖与稀硫酸共热后的溶液中,滴加银氨溶液,验证产物中的葡萄糖 | |
| E. | 用新制的银氨溶液可区分甲酸甲酯和乙醛 |
19.下列物质:①氯气 ②二氧化硫 ③活性炭 ④漂白粉,都能使品红溶液褪色,但褪色过程不发生氧化还原反应的是( )
| A. | ①② | B. | ②③ | C. | ①④ | D. | ②③④ |
3.下列叙述正确的是( )
| A. | 在原电池的负极和电解池的阴极上都是发生失电子的氧化反应 | |
| B. | 用惰性电极电解Na2SO4溶液,阴阳两极产物的物质的量之比为1:2 | |
| C. | 用惰性电极电解饱和KBr溶液,若有1 mol电子转移,则生成1 molKOH | |
| D. | 镀层破损后,镀锡铁板比镀锌铁板更耐腐蚀 |
4.常温下,将盐酸和一元碱BOH溶液等体积混合,两种溶液的物质的量浓度和混合溶液的pH如下表所示:
根据实验结果,回答下列问题:
(1)试写出BOH在溶液中的电离方程式:BOH?B++OH-
(2)甲组混合溶液中离子浓度由大到小的顺序为:c(Cl-)>c(B+)>c(H+)>c(OH-)
(3)乙组混合溶液中B-离子浓度c(B-)=0.05 mol/L
(4)丙组混合溶液中c(BOH)、c(B-)、c(Cl-)浓度大小关系为c(BOH)>c(B+)>c(Cl-)
(5)根据乙组实验,列式并计算BOH在常温下的电离平衡常数Kb=5×10-8.
| 实验序号 | HCl溶液浓度(mol/L) | BOH溶液溶液(mol/L) | 混合后溶液pH |
| 甲 | 0.10 | 0.10 | 4.7 |
| 乙 | 0.10 | 0.30 | 7 |
| 丙 | 0.10 | 0.50 | 8.2 |
(1)试写出BOH在溶液中的电离方程式:BOH?B++OH-
(2)甲组混合溶液中离子浓度由大到小的顺序为:c(Cl-)>c(B+)>c(H+)>c(OH-)
(3)乙组混合溶液中B-离子浓度c(B-)=0.05 mol/L
(4)丙组混合溶液中c(BOH)、c(B-)、c(Cl-)浓度大小关系为c(BOH)>c(B+)>c(Cl-)
(5)根据乙组实验,列式并计算BOH在常温下的电离平衡常数Kb=5×10-8.
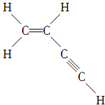 则分子中有7个 σ 键,3个 π 键.
则分子中有7个 σ 键,3个 π 键.