题目内容
下列叙述正确的是( )
| A、48 g O3气体含有6.02×1023个O3分子 |
| B、常温常压下,4.6 gNO2气体含有1.81×1023个NO2分子 |
| C、0.5 mol?L-1L CuCl2溶液中含有3.01×1023个Cu2+ |
| D、标准状况下,22.4 L氯气与足量氢氧化钠溶液反应转移的电子数为2NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A、根据n=
计算臭氧的物质的量,带入N=n?NA计算分子数;
B、根据n=
计算臭氧的物质的量,带入N=n?NA计算分子数;
C、铜离子在水中可以发生水解反应;
D、氯气与氢氧化钠溶液反应为歧化反应,转移电子数等于反应了的氯气分子数.
| m |
| M |
B、根据n=
| m |
| M |
C、铜离子在水中可以发生水解反应;
D、氯气与氢氧化钠溶液反应为歧化反应,转移电子数等于反应了的氯气分子数.
解答:
解:A、48 g O3气体的物质的量为
=1mol,所含有的分子数为1mol×6.02×1023mol-1=6.02×1023,故A正确;
B、4.6 gNO2气体的物质的量为0.1mol,含有的分子数为3.01×1023,故B错误;
C、铜离子在水中可以发生水解反应,因此溶液中的铜离子个数少于3.01×1023个,故C错误;
D、标准状况下,22.4L氯气的物质的量为1mol,氯气与氢氧化钠溶液反应为歧化反应,转移电子数为NA,故D错误;
故选A.
| 48g |
| 48g/mol |
B、4.6 gNO2气体的物质的量为0.1mol,含有的分子数为3.01×1023,故B错误;
C、铜离子在水中可以发生水解反应,因此溶液中的铜离子个数少于3.01×1023个,故C错误;
D、标准状况下,22.4L氯气的物质的量为1mol,氯气与氢氧化钠溶液反应为歧化反应,转移电子数为NA,故D错误;
故选A.
点评:本题考查了物质的量的有关计算,题目难度一般,特别注意氯气与氢氧化钠溶液反应转移电子数的计算.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
1.92g铜与足量一定浓度的硝酸反应,铜恰好全部溶解,生成气体896mL(标准状况),整个过程消耗硝酸的物质的量是( )
| A、0.08mol |
| B、0.12mol |
| C、0.10mol |
| D、0.09mol |
下列做法能改变溶液中溶质质量分数的是( )
| A、将氯化铵的饱和溶液降温 |
| B、将硝酸钾的饱和溶液升温 |
| C、把氯化钠的饱和溶液恒温蒸发 |
| D、在蔗糖的饱和溶液中再加少量蔗糖 |
高分子化合物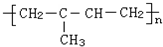 的单体是( )
的单体是( )
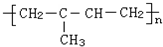 的单体是( )
的单体是( )| A、1,3-丁二烯 |
| B、2-甲基-1,3-丁二烯 |
| C、2-甲基-2-丁烯 |
| D、乙烯和丙烯 |
下列有关Cl、N、S等非金属元素化合物的说法正确的是( )
| A、漂白粉的成分为次氯酸钙 |
| B、实验室可用NaOH溶液处理SO2和Cl2废气 |
| C、实验室可用浓硫酸干燥氨气 |
| D、Al2(SO4)3可除去碱性废水及酸性废水中的悬浮颗粒 |
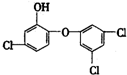 据报道,某牙膏中含有的消毒剂三氯生,遇含氯的自来水会生成哥罗芳(三氯甲烷),哥罗芳能导致肝病,甚至癌症.已知三氯生的结构简式如图所示,下列有关说法中不正确的是( )
据报道,某牙膏中含有的消毒剂三氯生,遇含氯的自来水会生成哥罗芳(三氯甲烷),哥罗芳能导致肝病,甚至癌症.已知三氯生的结构简式如图所示,下列有关说法中不正确的是( )| A、三氯生能与NaOH反应 |
| B、三氯生是一种芳香族化合物 |
| C、三氯生与NaHCO3作用可产生CO2气体 |
| D、哥罗芳没有同分异构体 |
下列性质的比较中,前者小于后者的是( )
| A、着火点:红磷与白磷 |
| B、密度:质量分数为20%的氨水与质量分数为20%的NaCl溶液 |
| C、氧化性:80%的硝酸与20%的硝酸 |
| D、熔点:二氧化硅和二氧化碳 |
下列叙述正确的是( )
| A、常温下干燥的Cl2能用钢瓶贮存 |
| B、14C可用于文物的年代鉴定,14C与12C互为同素异形体 |
| C、BaSO4 在医学上用作钡餐,Ba2+对人体无毒 |
| D、煤的干馏和石油的分馏均属化学变化 |