题目内容
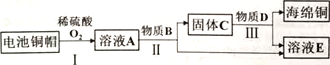
【题目】利用废旧电池铜帽(含Cu、Zn)制取海绵铜(Cu),并得到硫酸锌溶液的主要流程如下(反应条件己略去):
已知:2Cu+2H2SO4+O2![]() 2CuSO4+2H2O
2CuSO4+2H2O
下列说法不正确的是
A. 过程II中分离操作的名称为过滤,该操作过程中使用到的玻璃仪器有烧杯、漏斗、玻璃棒
B. 溶液A中的溶质有H2SO4、CuSO4、ZnSO4
C. 上述流程中加入的物质B为锌,物质D为盐酸
D. AE中含铜、锌两种元素的物质有A和C
【答案】C
【解析】通过分析转化流程可知,含Cu、Zn铜帽与稀硫酸和氧气反应生成了硫酸铜和硫酸锌的混合液A,依据实验的目的,为了得到铜和硫酸锌,应向A溶液加入过量的锌,通过过滤得到了硫酸锌溶液和铜锌的固体混合物C,为了得到铜和硫酸锌,应加入稀硫酸。
A、过滤的方法可以将固体和液体分离,过程Ⅱ中为了分离固体和液体,所以操作的名称是:过滤;过滤操作需要的玻璃仪器有:烧杯、漏斗、玻璃棒;故A正确;B、通过题中的反应流程可知,铜、氧气和硫酸会生成硫酸铜,硫酸和锌会生成硫酸锌,硫酸一般是过量的,所以溶液A中的溶质有:H2SO4、CuSO4、ZnSO4;故B正确;C、应向A溶液加入过量的锌,通过过滤得到了硫酸锌溶液和铜锌的固体混合物C,为了得到铜和硫酸锌,应加入稀硫酸,故C错误;D、通过上述分析可知,溶液A是硫酸铜和硫酸锌的混合物,固体C是铜和锌的混合物,所以含铜、锌两种元素的物质有:A、C,故D正确;故选C。

 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案 一线名师权威作业本系列答案
一线名师权威作业本系列答案【题目】下列各组物质中,不能满足表中图示物质在一定条件下一步转化关系的组合为
组别 | X | Y | Z | W |
|
A | Al | AlCl3 | Al(OH)3 | Al2O3 | |
B | Na | Na2O2 | Na2CO3 | NaCl | |
C | Fe | FeCl2 | FeCl3 | Fe(OH)3 | |
D | Si | Na2SiO3 | H2SiO3 | SiO2 |
A. A B. B C. C D. D