题目内容
16.下列电离方程式错误的是( )| A. | NaHCO3═Na++H++CO32- | B. | NaHSO4═Na++H++SO42- | ||
| C. | Fe(OH)3?Fe3++3OH- | D. | Ba(OH)2═Ba2++2OH- |
分析 A.碳酸氢根离子为弱酸的酸式根离子,不能拆;
B.硫酸氢钠为强电解质,水中完全电离出钠离子、氢离子、硫酸根离子;
C.氢氧化铁为弱电解质,部分电离用可逆号;
D.氢氧化钡为强电解质,完全电离.
解答 解:A.碳酸氢钠电离方程式:NaHCO3═Na++HCO3-,故A错误;
B.硫酸氢钠为强电解质,水中完全电离出钠离子、氢离子、硫酸根离子,电离方程式:NaHSO4═Na++H++SO42-,故B正确;
C.氢氧化铁为弱电解质,部分电离用可逆号,电离方程式:Fe(OH)3?Fe3++3OH-,故C正确;
D.氢氧化钡为强电解质,完全电离,电离方程式:Ba(OH)2═Ba2++2OH-,故D正确;
故选:A.
点评 本题考查了电解质电离方程式的书写,明确电解质强弱及电离方式是解题关键,注意碳酸氢根为弱酸的酸式根离子,不能拆,注意电离方程式遵循原子个数、电荷守恒规律,题目难度不大.

练习册系列答案
 挑战100单元检测试卷系列答案
挑战100单元检测试卷系列答案
相关题目
7.在密闭容器中发生如下反应:mA(g)+nB(g)?pC(g),达到平衡后,保持温度不变,将气体体积缩小到原来的一半,当达到新平衡时,C的浓度为原来1.8倍,下列说法错误的是( )
| A. | m+n<p | B. | 平衡向逆反应方向移动 | ||
| C. | A的转化率降低 | D. | C的体积分数增加 |
4.下列仪器不能用于加热的是( )
| A. | 容量瓶 | B. | 蒸馏烧瓶 | C. | 试管 | D. | 烧杯 |
11.下列离子方程式书写正确的是( )
| A. | 澄清石灰水跟过量CO2气体反应:Ca(OH)2+CO2=CaCO3↓+H2O | |
| B. | 稀硫酸与Cu反应:2H++Cu=Cu2++H2↑ | |
| C. | 腐蚀法制作印刷线路板:2Fe3++Cu=2Fe2++Cu2+ | |
| D. | 铁粉加入AgNO3溶液中:Fe+Ag+=Fe2++Ag |
1.遇到下列情况时,其处理方法有误的是( )
| A. | 将CO中毒者转移到通风处抢救 | |
| B. | 皮肤上不慎沾有浓碱液,立即用大量水冲洗,然后涂上2% 的硼酸溶液 | |
| C. | 少量酒精失火时,立即用湿抹布盖灭 | |
| D. | 夜间进入厨房,闻到很浓的煤气味,立即开灯检查 |
8.用已知浓度的酸滴定未知浓度的碱时,用甲基橙作指示剂,会导致待测碱液的浓度偏低的操作是( )
| A. | 滴定中不慎将锥形瓶内液体摇出少量于瓶外 | |
| B. | 锥形瓶用蒸馏水洗后,用待测夜润洗 | |
| C. | 酸式滴定管用蒸馏水洗后,未用标准液润洗 | |
| D. | 滴定前酸式滴定管尖嘴部分有气泡,滴定完成后气泡消失 |
5.一定条件下,CH3COONa溶液存在水解平衡:CH3COO-+H2OCH3COOH+OH-,下列说法正确的是( )
| A. | 加入少量NaOH固体,c(CH3COO-)增大 | |
| B. | 加入少量FeCl3固体,c(CH3 COO-)增大 | |
| C. | 稀释溶液,溶液的pH增大 | |
| D. | 加入适量醋酸得到的酸性混合溶液:c( Na+)>c(CH3COO-)>c(H+)>c( OH-) |
6.下列解释事实的化学方程式或离子方程式,不正确的是( )
| A. | 用FeSO4除去酸性废水中的Cr2O72-:Cr2O72-+6 Fe2++14H+═2Cr3++6 Fe3++7H2O | |
| B. | NH4Al(SO4)2溶液中加入少量的氢氧化钠溶液:Al3++3OH-═Al(OH)3↓ | |
| C. | 用惰性电极电解MgCl2溶液2H2O+2Cl-$\frac{\underline{\;电解\;}}{\;}$Cl2↑+H2↑+2OH- | |
| D. | 用CaSO4治理盐碱地:CaSO4(s)+Na2CO3(aq)?CaCO3(s)+Na2SO4(aq) |
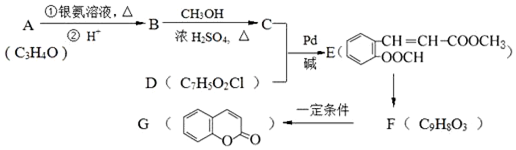

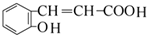 .
.
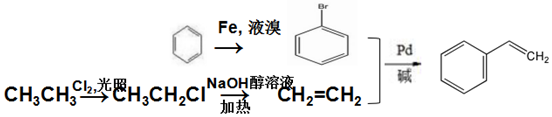 .
.