题目内容
下列晶体直接由原子构成的有( )
| A、硫磺 | B、石英晶体 |
| C、氩 | D、金属铝 |
考点:不同晶体的结构微粒及微粒间作用力的区别
专题:化学键与晶体结构
分析:根据原子晶体等由原子构成,有些物质是由分子构成的,如水、氢气等分子晶体,有些物质是由离子构成的,如氯化钠等离子晶体,金属晶体是由金属阳离子和自由电子构成,根据晶体类型进行分析判断即可.
解答:
解:A、硫磺属于分子晶体,晶体直接由分子构成,故A错误;
B、石英晶体属于原子晶体,是由原子直接构成的,故B正确;
C、氩是单原子构成的分子,是由原子直接构成的,故C正确;
D、金属铝是由铝离子和自由电子构成的,故D错误.
故选:BC.
B、石英晶体属于原子晶体,是由原子直接构成的,故B正确;
C、氩是单原子构成的分子,是由原子直接构成的,故C正确;
D、金属铝是由铝离子和自由电子构成的,故D错误.
故选:BC.
点评:本题考查了构成物质的微观粒子方面的知识,掌握常见物质的粒子构成是正确解答本题的关键,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
除去混在Na2CO3粉末中的少量NaHCO3最合理的方法是( )
| A、加热 |
| B、加NaOH溶液 |
| C、加盐酸 |
| D、加CaCl2溶液 |
N2O5是一种新型硝化剂,在一定温度下可发生以下反应:2N2O5(g)?4NO2 (g)+O2(g)△H>0
t℃时,向密闭容器中通入N2O5,部分实验数据见下表:下列说法中不正确的是( )
t℃时,向密闭容器中通入N2O5,部分实验数据见下表:下列说法中不正确的是( )
| 时间/s | 0 | 500 | 100 0 | 150 0 |
| c(N2O5)/mol?L-1 | 5.00 | 3.52 | 2.50 | 2.50 |
| A、500 s 内N2O5分解速率为2.96╳10-3mol?L-1?s-1 |
| B、达平衡时,N2O5的转化率为50% |
| C、达平衡后,升高温度平衡常数减小 |
| D、达平衡后,其他条件不变,将容器的体积压缩到原来的一半,c(N2O5)>5.00 mol?L-1 |
下列说法正确的是( )
| A、化合反应一定是放热反应 |
| B、乙二醇和丙三醇都易溶于水和乙醇 |
| C、牺牲阳极的阴极保护法是利用了电解原理 |
| D、相同条件下,CuSO4溶液比FeCl3溶液使H2O2分解速率更快 |
金属铊的盐类有剧毒,下列关于
Tl的说法正确的是( )
201 81 |
| A、质量数是120 |
| B、质子数是81 |
| C、电子数是120 |
| D、中子数是201 |
下列说法正确的是( )
①通过丁达尔效应可以鉴别稀豆浆和Fe(OH)3胶体
②常温时,FeCl3溶液中Fe3+与Cl-的个数之比等于1:3
③化学方程式Br2+2KI=2KBr+I2说明Br的非金属性强于I
④常温时,0.1mol?L-1盐酸中由水电离出的c(H+)<10-7mol?L-1.
①通过丁达尔效应可以鉴别稀豆浆和Fe(OH)3胶体
②常温时,FeCl3溶液中Fe3+与Cl-的个数之比等于1:3
③化学方程式Br2+2KI=2KBr+I2说明Br的非金属性强于I
④常温时,0.1mol?L-1盐酸中由水电离出的c(H+)<10-7mol?L-1.
| A、①② | B、③④ | C、①③ | D、②④ |
下列各化合物的命名正确的是( )
| A、CH2=CH-CH=CH2 1,3-二丁烯 |
B、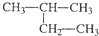 2-甲基丁烷 2-甲基丁烷 |
C、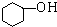 苯酚 苯酚 |
D、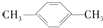 间二甲苯 间二甲苯 |
 今有某一种碱金属的两种碳酸盐和碱土金属(第ⅡA族)的一种不溶性碳酸盐组成的混合物,取其7.560g与过量盐酸完全反应,放出CO2体积为1.344L(标况下),另取等质量的原混合物,加水搅拌,可滤出不溶性盐1.420g.
今有某一种碱金属的两种碳酸盐和碱土金属(第ⅡA族)的一种不溶性碳酸盐组成的混合物,取其7.560g与过量盐酸完全反应,放出CO2体积为1.344L(标况下),另取等质量的原混合物,加水搅拌,可滤出不溶性盐1.420g.