题目内容
下列说法正确的是( )
| A、化合反应一定是放热反应 |
| B、乙二醇和丙三醇都易溶于水和乙醇 |
| C、牺牲阳极的阴极保护法是利用了电解原理 |
| D、相同条件下,CuSO4溶液比FeCl3溶液使H2O2分解速率更快 |
考点:吸热反应和放热反应,金属的电化学腐蚀与防护,化学反应速率的影响因素,醇类简介
专题:
分析:A.化合反应可能为吸热反应,也可能为放热反应;
B.乙二醇和丙三醇易溶于乙醇;
C.利用原电池原理的牺牲阳极的阴极保护法;
D.FeCl3是催化剂.
B.乙二醇和丙三醇易溶于乙醇;
C.利用原电池原理的牺牲阳极的阴极保护法;
D.FeCl3是催化剂.
解答:
解:A.碳与氧气的化合反应为放热反应,碳和二氧化碳的化合反应为吸热反应,故A错误;
B.乙二醇和丙三醇易溶于乙醇,也易溶于水,故B正确;
C.牺牲阳极的阴极保护法是利用原电池原理,故C错误;
D.FeCl3是催化剂,比硫酸铜催化效果好,故D错误.
故选B.
B.乙二醇和丙三醇易溶于乙醇,也易溶于水,故B正确;
C.牺牲阳极的阴极保护法是利用原电池原理,故C错误;
D.FeCl3是催化剂,比硫酸铜催化效果好,故D错误.
故选B.
点评:本题考查吸热反应、物质的溶解性、电解以及催化剂等,比较基础,侧重对基础知识的巩固,注意对基础知识的理解掌握.

练习册系列答案
 核心素养学练评系列答案
核心素养学练评系列答案 单元期中期末卷系列答案
单元期中期末卷系列答案
相关题目
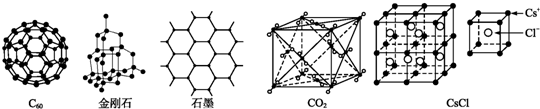
下列晶体直接由原子构成的有( )
| A、硫磺 | B、石英晶体 |
| C、氩 | D、金属铝 |
在一个1L的密闭容器中,加入2molA和1molB,发生下述反应:2A(g)+B(g)?3C(g)+D(g)达到平衡时,C的浓度为1.2mol/L,C的体积分数为a%.维持容器的体积和温度不变,按下列配比作为起始物质,达到平衡后,C的浓度仍是1.2mol/L的是( )
| A、6mol C+2mol D |
| B、1mol A+0.5mol B+1.5mol C+0.5mol D |
| C、1mol A+0.5mol B+1.5mol C |
| D、4mol A+2mol B |
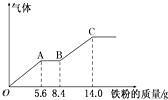 某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份.向其中一份中逐渐加入铜粉,最多能溶解9.6g.向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示(已知硝酸只被还原为NO气体).下列分析或结果错误的是( )
某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份.向其中一份中逐渐加入铜粉,最多能溶解9.6g.向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示(已知硝酸只被还原为NO气体).下列分析或结果错误的是( )| A、原混合酸中HNO3的物质的量为0.1 mol |
| B、OA段产生的是NO,AB段的反应为Fe+2Fe3+═3Fe2+,BC段产生氢气 |
| C、第二份溶液中最终溶质为FeSO4 |
| D、H2SO4浓度为2.5 mol?L-1 |
 某同学想利用镁与盐酸或醋酸在不同温度下反应,探究外界条件对反应速率的影响.部分实验用表如下:
某同学想利用镁与盐酸或醋酸在不同温度下反应,探究外界条件对反应速率的影响.部分实验用表如下: