��Ŀ����
����Ŀ�����Ļ������������������й㷺���ڡ�
��1�������ǽ�1mol�����������AB��Ϊ������̬ԭ��A��B�������������֪���л�ѧ���ļ������±���
![]()
д��1mol��̬��(H2N-NH2)ȼ�����ɵ�����ˮ�������Ȼ�ѧ����ʽ________________��
��2���ý�̿��ԭNO�ķ�ӦΪ��2NO(g)+C(s)![]() N2(g)+CO2(g)�����ݻ���Ϊ1L�ļס��ҡ����������ݺ���(��Ӧ�¶ȷֱ�Ϊ400�桢400�桢T��)�����зֱ���������Ľ�̿��һ������NO����ø�������n(NO)�淴Ӧʱ��t�ı仯������±���ʾ��
N2(g)+CO2(g)�����ݻ���Ϊ1L�ļס��ҡ����������ݺ���(��Ӧ�¶ȷֱ�Ϊ400�桢400�桢T��)�����зֱ���������Ľ�̿��һ������NO����ø�������n(NO)�淴Ӧʱ��t�ı仯������±���ʾ��
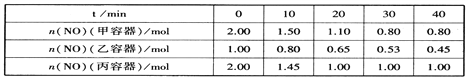
�ٸ÷�ӦΪ________(��������������������)��Ӧ��
����������60minʱ�ﵽƽ��״̬����0��60min����NO��Ũ�ȱ仯��ʾ��ƽ����Ӧ����v(NO)=____________��
��3���ý�̿��ԭNO2�ķ�ӦΪ��2NO2(g)+2C(s) ![]() N2(g)+2CO2(g)���ں��������£�1molNO2������C�����÷�Ӧ�����ƽ��ʱNO2��CO2�����ʵ���Ũ����ƽ����ѹ�Ĺ�ϵ��ͼ��ʾ��
N2(g)+2CO2(g)���ں��������£�1molNO2������C�����÷�Ӧ�����ƽ��ʱNO2��CO2�����ʵ���Ũ����ƽ����ѹ�Ĺ�ϵ��ͼ��ʾ��
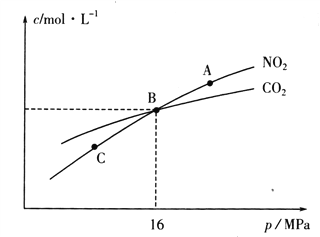
��A��C�����Ũ��ƽ�ⳣ����ϵ��Kc(A)________Kc(C)(����<������>������=��)��
��A��B��C������NO2��ת������ߵ���________(����A������B������C��)�㡣
�ۼ���B��ʱ�÷�Ӧ��ѹǿƽ�ⳣ��Kp(B)=________(Kp����ƽ���ѹ����ƽ��Ũ�ȼ��㣬��ѹ=��ѹ�����ʵ�������)��
���𰸡�![]() ���� 0.01mol/(L��min) �� C 3.2MPa
���� 0.01mol/(L��min) �� C 3.2MPa
��������
������1�������ʱ�=��Ӧ���ܼ��ܣ��������ܼ��ܼ���1mol��̬��(H2N-NH2)ȼ�����ɵ�����ˮ�������ʱ�����2�����Ƚϼס�����ͼ�����ݣ����ķ�Ӧ���ʴ��ڼף���֪�����¶ȴ���400�� ��ƽ��ʱ����NOŨ�ȴ��ڼף����������¶�ƽ�������ƶ���������![]() ���㷴Ӧ���ʣ���3����A��C�����¶���ͬ������ƽ�ⳣ����ȣ�������ѹǿƽ�������ƶ���������ƽ�ⳣ������ʽ����B��ʱ�÷�Ӧ��ѹǿƽ�ⳣ����
���㷴Ӧ���ʣ���3����A��C�����¶���ͬ������ƽ�ⳣ����ȣ�������ѹǿƽ�������ƶ���������ƽ�ⳣ������ʽ����B��ʱ�÷�Ӧ��ѹǿƽ�ⳣ����
��������1�������ʱ�=��Ӧ���ܼ��ܣ��������ܼ����� 1mol��̬��(H2N-NH2)ȼ�����ɵ�����ˮ�������ʱ�=193KJ/mol��391 KJ/mol��4��497 KJ/mol��946 KJ/mol��463 KJ/mol��4=��544 KJ/mol������1mol��̬��(H2N-NH2)ȼ�����ɵ�����ˮ�������Ȼ�ѧ����ʽ��![]() ��
��
��2�����Ƚϼס�����ͼ�����ݣ����ķ�Ӧ���ʴ��ڼף���֪�����¶ȴ���400�� ��ƽ��ʱ����NOŨ�ȴ��ڼף����������¶�ƽ�������ƶ�����������Ӧ������
��
��ƽ�ⳣ��=![]() �������¶���ͬ������ƽ�ⳣ����ͬ������װ��NO��Ũ�ȱ仯��Ϊxmol/L��
�������¶���ͬ������ƽ�ⳣ����ͬ������װ��NO��Ũ�ȱ仯��Ϊxmol/L��
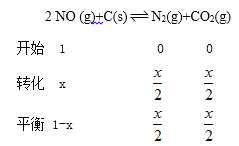
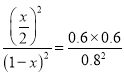 ��x=0.6������
��x=0.6������![]() ��v(NO)=
��v(NO)=![]() 0.01mol/(L��min)��
0.01mol/(L��min)��
��3����A��C�����¶���ͬ������ƽ�ⳣ���������Kc(A)=Kc(C)��������ѹǿƽ�������ƶ���NO2��ת������ߵ���C�������ݷ���ʽ��N2(g)��ƽ��Ũ����CO2Ũ�ȵ�![]() ������B��ʱ��NO2��N2��CO2���ʵ��������ֱ���
������B��ʱ��NO2��N2��CO2���ʵ��������ֱ���![]() ��
��![]() ��
��![]() �� B��ʱ�÷�Ӧ��ѹǿƽ�ⳣ��=
�� B��ʱ�÷�Ӧ��ѹǿƽ�ⳣ��=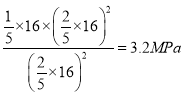 ��
��

����Ŀ���������ȣ�ClO2���㷺Ӧ����ֽ��Ư�ס�ɱ��������ˮ��������������ҵ�����ü״���ԭNaClO3�ķ����Ʊ�ClO2�������������£�
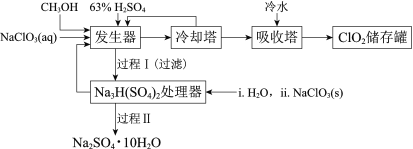
��֪��a�����������Ʊ�ClO2�ķ�Ӧ��12NaClO3+8H2SO4+3CH3OH= 12ClO2��+3HCOOH+4Na3H(SO4)2��+9H2O
b��������ʵ��۷е㣺
���� | CH3OH | HCOOH | ClO2 |
�۵�/�� | ��97 | 9 | ��59 |
�е�/�� | 65 | 101 | 11 |
(1)ClO2������ֽ��Ư�ס�ɱ���������������______�ԡ�
(2)��ȴ�����ڷ���ClO2������CH3OH��Ӧ���Ƶ�����¶�Ϊ______������ĸ����
A��0~10�� B��20~30�� C��60~70��
(3)�����̢���̢���Ի��â����Na2SO4��10H2O����ʹ����ԭ��ѭ�����á�
��֪��Na2SO4��10H2O��Na2SO4���ܽ����������ͼ��
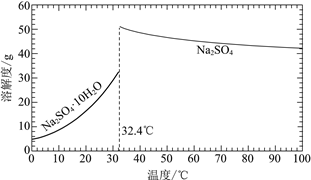
��Na3H(SO4)2�������л��â��ʱ�����NaClO3���壬��â���ܽ�ƽ��ĽǶȽ�����ԭ��______��
�ڽ��Na2SO4��10H2O��Na2SO4���ܽ�����ߣ����̢�IJ����ǣ���32.4�����������______��
��Na3H(SO4)2����������Һ�п���ѭ�����õ�ԭ����NaClO3��______��