题目内容
10.下列有关实验原理或实验操作正确的是( )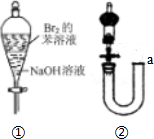
| A. | 在蒸发皿中灼烧CuSO4•5H2O晶体以除去结晶水 | |
| B. | 配制0.1 mol•L-1硫酸溶液时,容量瓶应先用0.1 mol•L-1硫酸溶液润洗 | |
| C. | 用图①所示装置实验,振荡后静置,溶液不再分层,且保持无色透明 | |
| D. | 沿图②中的a口加水,可以检验该装置的气密性. |
分析 A.灼烧固体应在坩埚中;
B.配制溶液时,容量瓶不能润洗;
C.溴与NaOH溶液反应后与苯分层;
D.从a处加水,左右两侧形成液面差.
解答 解:A.灼烧固体应在坩埚中,不能在蒸发皿中进行,蒸发皿用来溶液的蒸发结晶,故A错误;
B.配制溶液时,容量瓶不能润洗,否则配制溶液浓度偏大,故B错误;
C.溴与NaOH溶液反应后与苯分层,上层为苯,均为无色,故C错误;
D.从a处加水,左右两侧形成液面差,则可检验图b装置的气密性,故D正确;
故选D.
点评 本题考查化学实验方案的评价,为高频考点,涉及实验基本操作、混合物分离提纯及气体的制取,把握实验分析能力及反应原理为解答的关键,注意方案的合理性、操作性、评价性分析,题目难度不大.

练习册系列答案
相关题目
18.下列说法正确的是( )
| A. | 硫在空气中的燃烧产物是二氧化硫,在纯氧中的燃烧产物是三氧化硫 | |
| B. | 铜与浓硫酸反应产生二氧化硫,而锌与浓硫酸反应产生氢气 | |
| C. | 二氧化硅是酸性氧化物能和烧碱溶液反应 | |
| D. | 在常温下,浓硫酸不与铜反应,是因为铜被钝化 |
5.CH2OH(CHOH)4CHO是葡萄糖的结构简式,它不可能发生的化学反应是( )
| A. | 燃烧 | B. | 银镜反应 | ||
| C. | 水解反应 | D. | 与新制备的Cu(OH)2反应 |
15.已知NH4++AlO2-+2H2O=Al(OH)3↓+NH3•H2O,向含有等物质的量的NH4+、Al3+、H+混合溶液中,慢慢滴加NaOH溶液,直至过量,并不断搅拌,发生以下离子反应:
①H++OH-=H2O
②Al(OH)3+OH-=AlO2-+2H2O
③Al3++3OH-=Al(OH)3↓
④NH4++OH-=NH3•H2O.
先后顺序正确的是( )
①H++OH-=H2O
②Al(OH)3+OH-=AlO2-+2H2O
③Al3++3OH-=Al(OH)3↓
④NH4++OH-=NH3•H2O.
先后顺序正确的是( )
| A. | ①→②→③→④ | B. | ①→③→②→④ | C. | ①→③→④→② | D. | ①→④→②→③ |
2.化学与人类生产、生活密切相关,下列有关说法不正确的是( )
| A. | 节日燃放的烟花,就是碱金属以及锶、钡等金属化合物焰色反应所呈现的色彩 | |
| B. | 铝制饭盒不宜长时间存放酸性或碱性的食物 | |
| C. | 可以用ClO2、O2代替Cl2对自来水进行消毒 | |
| D. | 玛瑙饰物的主要成分与制造计算机芯片的主要成分相同 |
8.下列是四种物质的分离实验,已知X与NaOH溶液不反应,则关于X、Y、Z、W所代表的四种物质说法正确的是( )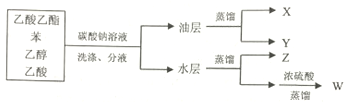

| A. | X是最简单的芳香烃,分子中含有三个碳碳双键 | |
| B. | Y是具有芳香气味的液体,难溶于水,易溶于有机溶剂,能发生水解反应 | |
| C. | Z是无色,有特殊香味的液体,与硫酸混合在140℃可以制备乙烯 | |
| D. | W是有强烈刺激性气味的无色液体,可与氢气发生加成反应,生成Z |