题目内容
18.下列说法正确的是( )| A. | 硫在空气中的燃烧产物是二氧化硫,在纯氧中的燃烧产物是三氧化硫 | |
| B. | 铜与浓硫酸反应产生二氧化硫,而锌与浓硫酸反应产生氢气 | |
| C. | 二氧化硅是酸性氧化物能和烧碱溶液反应 | |
| D. | 在常温下,浓硫酸不与铜反应,是因为铜被钝化 |
分析 A.硫与氧气反应生成二氧化硫;
B.浓硫酸有强氧化性;
C.二氧化硅与氢氧化钠反应生成硅酸钠和水;
D.常温下铜与浓硫酸不发生钝化.
解答 解:A.硫与氧气反应生成二氧化硫,得不到三氧化硫,故A错误;
B.浓硫酸有强氧化性,锌与浓硫酸反应不产生氢气,故B错误;
C.二氧化硅与氢氧化钠反应生成硅酸钠和水,能和烧碱溶液反应,故C正确;
D.常温下铜与浓硫酸不发生钝化,铜与浓硫酸常温下不反应是因为铜性质不活泼,故D错误;
故选C.
点评 本题考查了元素化合物知识,熟悉相关物质的化学性质是解题关键,注意铜与浓硫酸反应条件,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
9.NA为阿伏加德罗常数的值,下列说法错误的是( )
| A. | 4.6g 由NO2和N2O4组成的混合气体中含有的原子总数为0.3NA | |
| B. | 7.4g 丁醇中存在的共价键总数为1.3NA | |
| C. | 铁与稀硝酸反应时,生产0.1mol NO转移的电子数为0.3NA | |
| D. | 0.2 g $D_2^{16}O$中含有的质子数,中子数,电子数均为0.1NA |
6.下列说法不正确的是( )
| A. | 化石燃料蕴藏的能量来自远古时期生物体所吸收利用的太阳能 | |
| B. | 光-热转化是目前技术最成熟、成本最低廉、应用最广泛的利用太阳能形式 | |
| C. | 氢气之所以被称为“绿色能源”是因为它燃烧的产物不会污染环境 | |
| D. | 人类利用的能源都是通过化学反应获得的 |
10.下列有关实验原理或实验操作正确的是( )
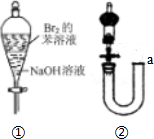

| A. | 在蒸发皿中灼烧CuSO4•5H2O晶体以除去结晶水 | |
| B. | 配制0.1 mol•L-1硫酸溶液时,容量瓶应先用0.1 mol•L-1硫酸溶液润洗 | |
| C. | 用图①所示装置实验,振荡后静置,溶液不再分层,且保持无色透明 | |
| D. | 沿图②中的a口加水,可以检验该装置的气密性. |
7.设NA为阿伏伽德罗常数的值.下列说法正确的是( )
| A. | 3.0g乙酸与甲酸甲酯的混合物中含有氧原子数目为0.2NA | |
| B. | 苯与液溴反应生成1mol溴苯分子,消耗0.5NA个Br2 | |
| C. | 常温常压下,等质量的N2H4和CH3OH含有相同数目的原子 | |
| D. | 6gSiO2晶体中含有0.4NA个Si-O键 |
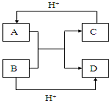 已知A、B、C、D是中学化学中常见的四种10电子微粒,它们之间存在如图中转化关系.
已知A、B、C、D是中学化学中常见的四种10电子微粒,它们之间存在如图中转化关系.