题目内容
下列说法正确的是( )
| A、明矾水解形成的Al(OH)3胶体能吸附水中悬浮物,可用于水的净化 |
| B、通电时,溶液中的溶质粒子分别向两极移动,胶体中的分散质粒子向某一极移动 |
| C、溶液中溶质粒子的运动有规律,胶体中分散质粒子的运动无规律,即布朗运动 |
| D、电解MgCl2饱和溶液,可制得金属镁 |
考点:胶体的重要性质
专题:溶液和胶体专题
分析:A.明矾中的铝离子水解生成氢氧化铝胶体,具有吸附悬浮杂质的作用;
B.通电时溶质电离出的阴阳离子分别移向两极,溶质是非电解质时不移向任何电极;
C.溶液中溶质分子运动无规律;
D.制取金属镁,应电解熔融氯化镁.
B.通电时溶质电离出的阴阳离子分别移向两极,溶质是非电解质时不移向任何电极;
C.溶液中溶质分子运动无规律;
D.制取金属镁,应电解熔融氯化镁.
解答:
解:A.明矾中的铝离子水解生成氢氧化铝胶体,具有吸附悬浮杂质的作用;可用于水的净化,故A正确;
B.通电时,溶液中的溶质粒子是电解质,电离出的阴阳离子分别向两极移动,若溶质是非电解质不移向电极,胶体中的分散质粒子向某一极移动,故B错误;
C.胶体的分散质粒子在显微镜观察下呈现无规则运动,这就是胶体的布朗运动特性.溶液中的离子呈现自由态,其运动是无规律可言的,故C错误;
D.制取金属镁,应电解熔融氯化镁,电解氯化镁溶液得到氢氧化镁沉淀和氢气,故D错误.
故选A.
B.通电时,溶液中的溶质粒子是电解质,电离出的阴阳离子分别向两极移动,若溶质是非电解质不移向电极,胶体中的分散质粒子向某一极移动,故B错误;
C.胶体的分散质粒子在显微镜观察下呈现无规则运动,这就是胶体的布朗运动特性.溶液中的离子呈现自由态,其运动是无规律可言的,故C错误;
D.制取金属镁,应电解熔融氯化镁,电解氯化镁溶液得到氢氧化镁沉淀和氢气,故D错误.
故选A.
点评:本题考查了胶体、溶液的性质区别和电解等,较简单,注意胶体粒子的吸附离子作用.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列叙述不正确的是( )
| A、提取碘水中的碘可采用加入四氯化碳后再分液的方法 |
| B、钨丝用于灯泡主要是因为钨的熔点很高 |
| C、胶体区别于其他分散系的本质特征是胶体能产生丁达尔现象 |
| D、生铁和钢的熔点都比纯铁低 |
下列用途主要是体现铝的物理性质的是( )
①家用铝锅 ②盛浓硝酸的容器 ③制导线 ④焊接钢轨 ⑤包装铝箔 ⑥制成合金作飞机制造业材料.
①家用铝锅 ②盛浓硝酸的容器 ③制导线 ④焊接钢轨 ⑤包装铝箔 ⑥制成合金作飞机制造业材料.
| A、只有①②③④ |
| B、只有④⑤⑥ |
| C、只有①③⑤⑥ |
| D、②④⑥ |
下列对化学反应的认识错误的是( )
| A、一定会伴随着化学键的变化 |
| B、不一定要遵循熵增加原理 |
| C、一定要遵循勒夏特勒原理 |
| D、一定要遵循能量守恒原理 |
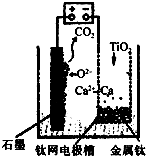 研究发现,可以用石墨作阳极、钛网作阴极、熔融CaF2-CaO作电解质,利用如图所示装置获得金属钙,并以钙为还原剂,还原二氧化钛制备金属钛.下列叙述正确的是( )
研究发现,可以用石墨作阳极、钛网作阴极、熔融CaF2-CaO作电解质,利用如图所示装置获得金属钙,并以钙为还原剂,还原二氧化钛制备金属钛.下列叙述正确的是( )| A、该电池工作过程中O2-向阴极移动 |
| B、阳极的电极反应式为C+2O2--4e-═CO2↑ |
| C、若用铅蓄电池作该装置的供电电源,“-”接线柱应连接PbO2电极 |
| D、在制备金属钛前后,整套装置中CaO的总量减少 |
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
A、由水电离的c(H+)=1×l0-12 mol?L-1的溶液中:Ba2+、K+、Cl-、NO
| ||||
B、1.0mol?L-1的KNO3溶液:H+、Fe2+、Cl-、SO
| ||||
C、无色溶液中:K+、Na+、MnO
| ||||
D、含有大量HCO
|
下列反应的离子方程式错误的是( )
| A、氯气通入氢氧化钠溶液中 Cl2+2OH-=Cl-+ClO-+H2O |
| B、澄清石灰水中通入过量二氧化碳:Ca2++2OH-+CO2═CaCO3↓+H2O |
| C、在硅酸钠溶液中滴加稀硫酸SiO32-+2H+=H2SO3↓ |
| D、二氧化硅与烧碱溶液反应:SiO2+2OH-═SiO32-+H2O |