题目内容
下列用途主要是体现铝的物理性质的是( )
①家用铝锅 ②盛浓硝酸的容器 ③制导线 ④焊接钢轨 ⑤包装铝箔 ⑥制成合金作飞机制造业材料.
①家用铝锅 ②盛浓硝酸的容器 ③制导线 ④焊接钢轨 ⑤包装铝箔 ⑥制成合金作飞机制造业材料.
| A、只有①②③④ |
| B、只有④⑤⑥ |
| C、只有①③⑤⑥ |
| D、②④⑥ |
考点:铝的化学性质,金属的通性
专题:几种重要的金属及其化合物
分析:不需要发生化学变化体现的性质,为物理性质,如密度、延展性、熔沸点、导电、导热性等,以此来解答.
解答:
解:①家用铝锅与导热性有关,体现物理性质;
②盛浓硝酸的容器,发生钝化,体现化学性质;
③制导线与导电性有关,体现物理性质;
④焊接钢轨,发生铝热反应,体现化学性质;
⑤包装铝箔,与延展性有关,体现物理性质;
⑥制成合金作飞机制造业材料,与其密度、熔点有关,体现物理性质,
故选C.
②盛浓硝酸的容器,发生钝化,体现化学性质;
③制导线与导电性有关,体现物理性质;
④焊接钢轨,发生铝热反应,体现化学性质;
⑤包装铝箔,与延展性有关,体现物理性质;
⑥制成合金作飞机制造业材料,与其密度、熔点有关,体现物理性质,
故选C.
点评:本题考查Al的性质,为高频考点,把握物理性质的判断及常见的物理性质即可解答,注重基础知识的考查,题目难度不大.

练习册系列答案
相关题目
下列实验方法或结论中,不正确的是( )
| A、用焰色反应即可鉴别KCl和Na2SO4二种物质 |
| B、实验室通常用氢氧化钠溶液来吸收多余的氯气尾气 |
| C、SO2与某些有色物质反应生成无色不稳定物质,可用于漂白纸浆等 |
| D、Na2CO3水溶液呈碱性,所以可用于治疗胃酸过多 |
关于酸、碱、盐的下列各种说法中,正确的是( )
| A、化合物电离时,生成的阳离子有氢离子的是酸 | ||
| B、化合物电离时,生成的阴离子有氢氧根离子的是碱 | ||
C、NH4Cl电离的电离方程式是:NH4Cl=NH
| ||
| D、化合物电离时,生成金属阳离子(或铵根离子)和酸根离子的是盐 |
aXn-和bYm+两种简单离子,其电子层结构相同,下列关系式或化学式正确( )
| A、a-n=b+m |
| B、a+m=b+n |
| C、氧化物为YOm |
| D、氢化物为HnX或XHn |
符合如图阴影部分的物质是( )
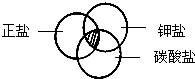

| A、NaCl |
| B、KHCO3 |
| C、K2CO3 |
| D、Na2CO3 |
在一密闭容器中盛有2molNa2O2与2molNaHCO3,将其加热到150℃,经充分反应后,容器内残留的固体是( )
| A、只有2molNaOH |
| B、2molNa2CO3和2molNaOH |
| C、2molNa2CO3和1molNa2O2 |
| D、只有2molNa2CO3 |
按C、N、O、F的顺序,下列递变规律错误的是( )
| A、原子半径逐渐减小 |
| B、元素原子得电子能力逐渐增强 |
| C、最高正化合价逐渐增大 |
| D、气态氢化物稳定性逐渐增大 |
下列说法正确的是( )
| A、明矾水解形成的Al(OH)3胶体能吸附水中悬浮物,可用于水的净化 |
| B、通电时,溶液中的溶质粒子分别向两极移动,胶体中的分散质粒子向某一极移动 |
| C、溶液中溶质粒子的运动有规律,胶体中分散质粒子的运动无规律,即布朗运动 |
| D、电解MgCl2饱和溶液,可制得金属镁 |