题目内容
2.对于下列反应的反应类型的判断,不正确的是( )| A. | CO2+H2O═H2CO3化合反应 | |
| B. | Cu2(OH)2CO3═2CuO+H2O+CO2↑ 分解反应 | |
| C. | CuO+CO═Cu+CO2 置换反应 | |
| D. | NaCl+AgNO3═AgCl↓+NaNO3复分解反应 |
分析 A.化合反应是有两种或两种以上的物质生成一种物质的化学反应,特征是:多变一;
B.分解反应是一变多;
C.置换反应是一种单质和一种化合物反应生成另一种单质和另一种化合物的化学反应;
D.复分解反应是两种化合物互相交换成分生成另外两种化合物的反应.
解答 解:A.CO2+H2O═H2CO3只生成一种物质是化合反应,故A正确;
B.Cu2(OH)2CO3═2CuO+H2O+CO2↑ 一种物质生成多种物质是分解反应,故B正确;
C.CuO+CO═Cu+CO2没有单质反应,不是置换反应,故C错误;
D.NaCl+AgNO3═AgCl↓+NaNO3是在溶液中交换离子的反应属于复分解反应,故D正确.
故选C.
点评 本题考查化学基本反应类型,题目难度不大,要加强记忆有关的知识点,并理解应用.

练习册系列答案
相关题目
10.已知m mol某气体的质量为a g,则 b g该气体在标准状况下的体积(L)为( )
| A. | 22.4am/b | B. | 22.4b/am | C. | 22.4bm/a | D. | 22.4a/bm |
14.下列离子方程式中书写正确的是( )
| A. | Fe跟FeCl3溶液反应:Fe+Fe3+═2Fe2+ | |
| B. | Fe跟稀硫酸反应:2Fe+6H+═2Fe3++3H2↑ | |
| C. | FeCl3与Cl2反应:Fe2++Cl2═Fe3++2Cl- | |
| D. | Fe(OH)3跟硝酸反应:Fe(OH)3+3H+═Fe3++3H2O |
6.在T℃时,向1L固定体积的密闭容器M中加入2mol X和1mol Y,发生如下反应:2X(g)+Y(g)?aZ(g)+W(g)△H=-Q kJ/mol(Q>0);该反应达到平衡后,放出的热量为Q1kJ,物质X的转化率为α;若平衡后再升高温度,混合气体的平均相对分子质量减小.
请回答下列问题:
(1)化学计量数a的值为1.
(2)下列能说明该反应达到了化学平衡状态的是ac(填序号).
a.容器内气体的压强一定b.容器内气体的密度一定
c.容器内Z的分子数一定d.容器内气体的质量一定
(3)维持T℃温度不变,若起始时向容器M中加入2mol X、1mol Y和1mol Ar(稀有气体不参与反应),则反应达到平衡后放出的热量是Q1kJ.若起始时向容器M中加入4mol X和6mol Y,反应达到平衡时容器内的分子数目减少10%,则反应中放出的热量为QkJ.
(4)维持T℃温度不变,若在一个和原容器体积相等的恒压容器N中加入2mol X和1mol Y,发生题给反应并达到平衡,则N(填“M”或“N”)容器中的反应先达到平衡状态,容器中X的质量分数M>N(填“>”、“<”或“=”).
(5)已知:该反应的平衡常数随温度的变化情况如表所示:
若在某温度下,2mol X和1mol Y在容器M中反应并达到平衡,X的平衡转化率为50%,则该温度为350℃.
请回答下列问题:
(1)化学计量数a的值为1.
(2)下列能说明该反应达到了化学平衡状态的是ac(填序号).
a.容器内气体的压强一定b.容器内气体的密度一定
c.容器内Z的分子数一定d.容器内气体的质量一定
(3)维持T℃温度不变,若起始时向容器M中加入2mol X、1mol Y和1mol Ar(稀有气体不参与反应),则反应达到平衡后放出的热量是Q1kJ.若起始时向容器M中加入4mol X和6mol Y,反应达到平衡时容器内的分子数目减少10%,则反应中放出的热量为QkJ.
(4)维持T℃温度不变,若在一个和原容器体积相等的恒压容器N中加入2mol X和1mol Y,发生题给反应并达到平衡,则N(填“M”或“N”)容器中的反应先达到平衡状态,容器中X的质量分数M>N(填“>”、“<”或“=”).
(5)已知:该反应的平衡常数随温度的变化情况如表所示:
| 温度/℃ | 200 | 250 | 300 | 350 |
| 平衡常数K | 9.94 | 5.2 | 1 | 0.5 |
7.设NA为阿伏伽德罗常数的值,下列有关说法不正确的是( )
| A. | 36g水中含有的水分子数是2NA | |
| B. | 标准状况下,33.6LCO中含有的原子数是3NA | |
| C. | 0.5L0.2mol/L的NaCl溶液中含有的Na+数是0.1NA | |
| D. | 常温常压下,1molCH4的体积约为22.4L |
 .
.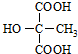 (或
(或 ).
).