题目内容
如图中A~J均为中学化学中常见的物质,它们之间有如下转化关系.其中A元素在元素周期表中位于第三周期ⅢA族,B为铁锈是主要成分,D为过渡元素金属单质.(反应过程中生成的水及其他产物已略去)

请回答以下问题:
(1)C是 ,H是 .(填化学式)
(2)A与B反应的化学方程式
(3)E与NaOH溶液反应生成F的离子方程式
(4)J与D反应转化为G的离子方程式 .

请回答以下问题:
(1)C是
(2)A与B反应的化学方程式
(3)E与NaOH溶液反应生成F的离子方程式
(4)J与D反应转化为G的离子方程式
考点:无机物的推断
专题:推断题
分析:I为红褐色固体,则I为Fe(OH)3,加热分解生成B,B为铁锈是主要成分,为Fe2O3,I与盐酸反应生成J,则J为FeCl3.D与J反应生成G,G与氢氧化钠反应生成H,H在空气中转化为氢氧化铁,则H为Fe(OH)2.A元素在元素周期表中位于第三周期ⅢA族,应为Al,A与B的反应生成C与D,则C为金属氧化物,与氢氧化钠反应,与盐酸反应,则C为Al2O3,D为Fe,则G为FeCl2,结合转化关系可知E为AlCl3,F为NaAlO2,以此解答该题.
解答:
解;I为红褐色固体,则I为Fe(OH)3,加热分解生成B,B为铁锈是主要成分,为Fe2O3,I与盐酸反应生成J,则J为FeCl3.D与J反应生成G,G与氢氧化钠反应生成H,H在空气中转化为氢氧化铁,则H为Fe(OH)2.A元素在元素周期表中位于第三周期ⅢA族,应为Al,A与B的反应生成C与D,则C为金属氧化物,与氢氧化钠反应,与盐酸反应,则C为Al2O3,D为Fe,则G为FeCl2,结合转化关系可知E为AlCl3,F为NaAlO2,
(1)由以上分析可知C为Al2O3,H为,故答案为:Al2O3;Fe(OH)2;
(2)A和B的反应的化学方程式为2Al+Fe2O3
Al2O3+2Fe,故答案为:2Al+Fe2O3
Al2O3+2Fe;
(3)E为AlCl3,与过量氢氧化钠反应生成NaAlO2,反应的离子方程式为Al3++4OH-=AlO2-+2H2O,故答案为:Al3++4OH-=AlO2-+2H2O;
(4)J与D反应转化为G的离子方程式为2Fe3++Fe=3Fe2+,故答案为:2Fe3++Fe=3Fe2+.
(1)由以上分析可知C为Al2O3,H为,故答案为:Al2O3;Fe(OH)2;
(2)A和B的反应的化学方程式为2Al+Fe2O3
| ||
| ||
(3)E为AlCl3,与过量氢氧化钠反应生成NaAlO2,反应的离子方程式为Al3++4OH-=AlO2-+2H2O,故答案为:Al3++4OH-=AlO2-+2H2O;
(4)J与D反应转化为G的离子方程式为2Fe3++Fe=3Fe2+,故答案为:2Fe3++Fe=3Fe2+.
点评:本题考查无机物的推断,为高频考点,综合考查元素化合物知识,把握铝热反应及两性化合物的性质为解答的关键,侧重Al、Fe及其化合物之间转化反应的考查,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列各组数据中,前者刚好是后者两倍的是( )
| A、2 mol水的摩尔质量和1 mol水的摩尔质量 |
| B、200 mL 1 mol/L氯化钙溶液中c(Cl-)和100 mL 2 mol/L氯化钾溶液中c(Cl-) |
| C、64 g二氧化硫中氧原子数和标准状况下22.4 L一氧化碳中氧原子数 |
| D、20%NaOH溶液中NaOH的物质的量浓度和10%NaOH溶液中NaOH的物质的量浓度 |
下列说法正确的是( )
| A、需要加热的反应一定是吸热反应 |
| B、所有的化学反应都有能量变化 |
| C、所有的放热反应都可以在常温常压下自发进行 |
| D、核能作为一种反应热,是理想的新能源 |
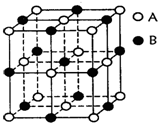 某微观模型如图所示,则下列说法正确的是( )
某微观模型如图所示,则下列说法正确的是( )| A、若该模型为一种气态团簇分子,则其分子式为A13B14 | ||
| B、若该模型为某离子晶体的晶胞,则该晶体的化学式为A4B4 | ||
C、若该模型为某纳米材料的颗粒,则该颗粒表面粒子占粒子总数的
| ||
| D、若该模型为某晶体的晶胞,晶胞中B原子位于最近且等距离A原子围成的正四面体空隙中心 |
有关晶体的结构如下图所示,下列说法中不正确的是( )
A、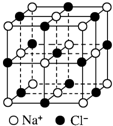 在NaCl晶体中,距Na+最近的Cl-形成正八面体 |
B、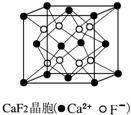 在CaF2晶体中,每个晶胞平均占有4个Ca2+ |
C、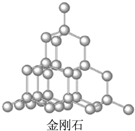 在金刚石晶体中,碳原子与碳碳键个数的比为1:4 |
D、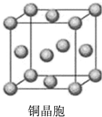 铜晶体为面心立方堆积,铜原子的配位数为12 |
 四种元素A、B、C、D位于元素周期表的前四周期,已知它们的核电荷数依次增加,且核电荷数之和为50;A元素原子的核外只有一个电子;B元素原子的L层p轨道中有2个电子;C元素原子与B元素原子的价层电子数相同;D原子的最外层电子数为1,其d轨道中的电子数与K层电子数之比为5:1.
四种元素A、B、C、D位于元素周期表的前四周期,已知它们的核电荷数依次增加,且核电荷数之和为50;A元素原子的核外只有一个电子;B元素原子的L层p轨道中有2个电子;C元素原子与B元素原子的价层电子数相同;D原子的最外层电子数为1,其d轨道中的电子数与K层电子数之比为5:1.