题目内容
人工肾脏可用间接电化学方法除去代谢产物中的尿素,原理如图.下列有关说法正确的是( )

| A、a为电源的负极 |
| B、电解结束后,阴极室溶液的pH与电解前相比将升高 |
| C、阳极室中发生的电极反应为2H++2e-=H2↑ |
| D、若两极共收集到气体13.44L(标准状况),则除去的尿素为7.2g(忽略气体的溶解) |
考点:电解原理
专题:
分析:A、根据电解池中阴离子在阳极放电和阳离子在阴极放电的规律,结合本题图中的电极产物CO2和N2可以判断出A为电源的正极,b为电源的负极;
B、阴极反应为:6H2O+6e-═6OH-+3H2↑(或6H++6e-═3H2↑)阳极反应为:6Cl--6e-═3Cl2↑,CO(NH2)2+3Cl2+H2O═N2+CO2+6HCl,根据上述反应式可以看出在阴、阳极上产生的OH-、H+的数目相等,阳极室中反应产生的H+通过质子交换膜进入阴极室与OH-恰好反应生成水,所以阴极室中电解前后溶液的pH不变;
C、由图可知,阳极室首先是氯离子放电生成氯气,氯气再氧化尿素生成氮气、二氧化碳,同时会生成HCl;
D、根据n=
计算两极产生的气体的物质的量,利用气体中各组分的比例关系,计算n(N2)=n(CO2),再根据方程式计算尿素的物质的量,根据m=nM计算尿素的质量.
B、阴极反应为:6H2O+6e-═6OH-+3H2↑(或6H++6e-═3H2↑)阳极反应为:6Cl--6e-═3Cl2↑,CO(NH2)2+3Cl2+H2O═N2+CO2+6HCl,根据上述反应式可以看出在阴、阳极上产生的OH-、H+的数目相等,阳极室中反应产生的H+通过质子交换膜进入阴极室与OH-恰好反应生成水,所以阴极室中电解前后溶液的pH不变;
C、由图可知,阳极室首先是氯离子放电生成氯气,氯气再氧化尿素生成氮气、二氧化碳,同时会生成HCl;
D、根据n=
| V |
| 22.4 |
解答:
解:A、由图可知,左室电极产物为CO2和N2,发生氧化反应,故A为电源的正极,右室电解产物H2,发生还原反应,故b为电源的负极,故A错误;
B、阴极反应为6H2O+6e-═6OH-+3H2↑(或6H++6e-═3H2↑),阳极反应为6Cl--6e-═3Cl2↑,CO(NH2)2+3Cl2+H2O═N2+CO2+6HCl,根据上述反应式可以看出在阴、阳极上产生的OH-、H+的数目相等,阳极室中反应产生的H+通过质子交换膜进入阴极室与OH-恰好反应生成水,所以阴极室中电解前后溶液的pH不变,故B错误;
C、由图可知,阳极室首先是氯离子放电生成氯气,氯气再氧化尿素生成氮气、二氧化碳,同时会生成HCl,阳极室中发生的反应依次为:2Cl--2e-═Cl2↑,CO(NH2)2+3Cl2+H2O═N2+CO2+6HCl,故C错误;
D、电解收集到的13.44L气体,物质的量为
=0.6mol,由反应CO(NH2)2+3Cl2+H2O═N2+CO2+6HCl可知n(N2)=n(CO2)=0.6mol×
=0.12 mol,
可知生成0.12mol N2所消耗的CO(NH2)2的物质的量也为0.12mol,其质量为:m[CO(NH2)2]=0.12 mol×60 g?mol-1=7.2g,故D正确;
故选:D.
B、阴极反应为6H2O+6e-═6OH-+3H2↑(或6H++6e-═3H2↑),阳极反应为6Cl--6e-═3Cl2↑,CO(NH2)2+3Cl2+H2O═N2+CO2+6HCl,根据上述反应式可以看出在阴、阳极上产生的OH-、H+的数目相等,阳极室中反应产生的H+通过质子交换膜进入阴极室与OH-恰好反应生成水,所以阴极室中电解前后溶液的pH不变,故B错误;
C、由图可知,阳极室首先是氯离子放电生成氯气,氯气再氧化尿素生成氮气、二氧化碳,同时会生成HCl,阳极室中发生的反应依次为:2Cl--2e-═Cl2↑,CO(NH2)2+3Cl2+H2O═N2+CO2+6HCl,故C错误;
D、电解收集到的13.44L气体,物质的量为
| 13.44L |
| 22.4L/mol |
| 1 |
| 5 |
可知生成0.12mol N2所消耗的CO(NH2)2的物质的量也为0.12mol,其质量为:m[CO(NH2)2]=0.12 mol×60 g?mol-1=7.2g,故D正确;
故选:D.
点评:本题考查电解池原理与有关计算,难度较大,关键注意观察电极产物,判断发生的反应,注意根据方程式判断左室中pH值的变化.

练习册系列答案
 学习实践园地系列答案
学习实践园地系列答案
相关题目
铟产业被称为“信息时代的朝阳产业”.元素周期表中铟的数据见图,下列说法完全正确的是( )


| A、铟元素的质量数是114.8 |
| B、铟元素的相对原子质量是115,中子数为66 |
| C、铟元素是一种主族元素,位于第五周期第ⅢA族 |
| D、铟原子最外层有3个能量相同的电子 |
下列有关能量的判断或表示方法正确的是( )
| A、从C(石墨)=C(金刚石)△H=1.9 kJ?mol-1,可知金刚石比石墨更稳定 |
| B、等质量的硫蒸气和硫固体分别完全燃烧,后者放出热量更多 |
| C、由H+(aq)+OH-(aq)=H2O(l)△H=-57.3 kJ?mol-1,则向含0.1 mol HCl的盐酸中加入4.0gNaOH固体,放出热量等于5.73 kJ |
| D、同一个化学反应,化学计量数不同,△H的值不同;化学计量数相同而状态不同,△H的值也不同 |
检验溶液中是否有S2O32-的一种方法:取待测液,向其中逐滴滴加硝酸银溶液,如果有S2O32-,会发生如下反应:
Ag++2S2O32-→[Ag(S2O3)2]3- 3Ag++[Ag(S2O3)2]3-→2Ag2S2O3↓(白色)
Ag2S2O3+H2O→Ag2S↓(黑色)+H2SO4下列叙述正确的是( )
Ag++2S2O32-→[Ag(S2O3)2]3- 3Ag++[Ag(S2O3)2]3-→2Ag2S2O3↓(白色)
Ag2S2O3+H2O→Ag2S↓(黑色)+H2SO4下列叙述正确的是( )
| A、此实验可在酸性溶液中进行 |
| B、此实验可在碱性溶液中进行 |
| C、此实验只能在中性溶液中进行 |
| D、硝酸银溶液必须过量 |
下列有机物命名正确的是( )
A、 2-乙基丙烷 2-乙基丙烷 |
B、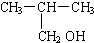 2-甲基丙醇 2-甲基丙醇 |
C、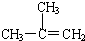 2-甲基丙烯 2-甲基丙烯 |
D、 2,2-二甲基-3-丁醇 2,2-二甲基-3-丁醇 |
下列关于核外电子的描述中,正确的是( )
| A、电子云图中一个小黑点表示一个电子 |
| B、电子式中元素符号周围的小黑点数表示核外电子总数 |
| C、s电子在s电子云的球形空间内做规则运动 |
| D、核外电子的能量大小主要是由电子层和电子亚层决定 |
某同学为检验溶液中是否含有常见的几种离子,进行了如图所示的实验操作.其中,检验过程中产生的气体能使湿润的红色石蕊试纸变蓝.由该实验能得到的正确结论是( )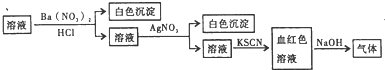

| A、原溶液中一定含有SO42- |
| B、原溶液中不一定含有NH4+ |
| C、原溶液中一定含有Cl- |
| D、原溶液中含Fe2+、Fe3+至少有一种 |
相同条件下等物质的量浓度的下列溶液,c(H+)浓度最大的是( )
| A、HCl |
| B、H2SO3 |
| C、H3PO4 |
| D、CH3COOH |