题目内容
10.设NA表示阿伏加德罗常数,下列叙述中正确的是( )| A. | 56gFe与足量的盐酸反应,转移的电子数为2NA | |
| B. | 标准状况下,22.4L的水中含有的原子数为3NA | |
| C. | 物质的量浓度为2mol/L的BaCl2溶液中,含有Cl-个数为4NA | |
| D. | 22.4 L CO和CO2的混合气体中所含的碳原子数一定是NA |
分析 A、求出铁的物质的量,然后根据铁和盐酸反应后变为+2价来分析;
B、标况下水为液体;
C、溶液体积不明确;
D、气体所处的状态不明确.
解答 解:A、56g铁的物质的量为1mol,而铁和盐酸反应后变为+2价,故1mol铁反应转移2NA个电子,故A正确;
B、标况下水为液体,故不能根据气体摩尔体积来计算其物质的量,故B错误;
C、溶液体积不明确,故溶液中的氯离子的个数无法计算,故C错误;
D、气体所处的状态不明确,故气体的物质的量无法计算,故D错误.
故选A.
点评 本题考查了阿伏伽德罗常数的有关计算,掌握物质的量的计算公式和物质结构是解题关键,难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
20.室温下,在一定体积pH=12的Ba(OH)2溶液中逐滴加入一定物质的量浓度的NaHSO4溶液,当溶液中的Ba2+恰好完全沉淀时,溶液pH=11.若体积可以加和,则V(Ba(OH)2):V( NaHSO4)为( )
| A. | 1:1 | B. | 1:2 | C. | 1:3 | D. | 1:4 |
18.以下化学用语及对应表达正确的是( )
| A. | H218O 的摩尔质量为20g?mol-1 | |
| B. | 铁粉溶于盐酸的化学方程式:2Fe+6HCl=2FeCl3+3H2↑ | |
| C. | 氯离子的结构示意图: | |
| D. | 乙醇的分子式为CH3CH2OH |
5.下列各种描述中,正确的是( )
| A. | 绿色食品是不含任何化学物质的食品 | |
| B. | 加碘食盐中所加的“碘”一般是碘化钾或碘单质 | |
| C. | 区别氯化铁溶液和氢氧化铁胶体可以用丁达尔效应 | |
| D. | 用干燥的有色布条可以检验氯化氢气体中是否混有氯气 |
15.下列有关物质的性质与用途具有对应关系的是( )
| A. | SO2具有还原性,可用于漂白纸浆 | |
| B. | NH4HCO3受热易分解,可用作氮肥 | |
| C. | 氢氧化铝具有弱碱性,可用作净水剂 | |
| D. | 常温下铁能被浓硝酸钝化,可用铁质容器贮运浓硝酸 |
2.己知反应A(g)+B(g)?C(g)+D(g)的平衡常数K值与温度的关系如表所示.830℃时,向一个2L的密闭容器中充入0.20molA和0.80molB,4s内v(A)=0.005mol•L-1•S-1.下列说法正确的是( )
| 温度/℃ | 700 | 830 | 1200 |
| K值 | 1.7 | 1.0 | 0.4 |
| A. | 4s时,c(B)为0.76 mol•L-1 | |
| B. | 830℃到平衡时,A的转化率为80% | |
| C. | 达平衡时,升高温度,平衡正向移动 | |
| D. | 1200℃时反应C(g)+D(g)?A(g)+B(g)的平衡常数的值为0.4 |

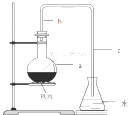 中学实验室用如图所示装置制取少量溴苯.请填写下列空白.
中学实验室用如图所示装置制取少量溴苯.请填写下列空白.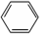 +Br2$\stackrel{FeBr_{3}}{→}$
+Br2$\stackrel{FeBr_{3}}{→}$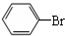 +HBr.
+HBr.