题目内容
下列说法正确的是( )
| A、强电解质一定是离子化合物,弱电解质一定是共价化合物 |
| B、强电解质一定是易溶化合物,弱电解质一定是难溶化合物 |
| C、SO3溶于水后水溶液导电性很强,所以SO3是强电解质 |
| D、属于共价化合物的电解质在熔化状态下一般不导电 |
考点:强电解质和弱电解质的概念
专题:电离平衡与溶液的pH专题
分析:A、强电解质是指在水溶液中,或熔融状态下能完全电离的化合物,弱电解质在水溶液中部分电离的电解质;
B、硫酸钡难溶于水,但它是强电解质,乙酸易溶于水,但它是弱酸,属于弱电解质;
C、三氧化硫不电离,三氧化硫和水反应生成硫酸,硫酸导电;
D、共价化合物是指:以共用电子对形成分子的化合物,没有离子存在.
B、硫酸钡难溶于水,但它是强电解质,乙酸易溶于水,但它是弱酸,属于弱电解质;
C、三氧化硫不电离,三氧化硫和水反应生成硫酸,硫酸导电;
D、共价化合物是指:以共用电子对形成分子的化合物,没有离子存在.
解答:
解:A、强电解质不一定是离子化合物,如氯化氢是共价化合物,但它在水溶液中能完全电离,它是强电解质,故A错误;
B、强弱电解质和溶于水的电解质是否完全电离有关,与是否难易溶于水无关.硫酸钡难溶于水,但它是强电解质,乙酸易溶于水,但它是弱酸,故B错误;
C、SO3溶于水和水结合成硫酸,硫酸是强电解质,三氧化硫是非电解质,故C错误;
D、共价化合物只存在分子,在熔融状态下,没有离子不导电,故D正确;
故选D.
B、强弱电解质和溶于水的电解质是否完全电离有关,与是否难易溶于水无关.硫酸钡难溶于水,但它是强电解质,乙酸易溶于水,但它是弱酸,故B错误;
C、SO3溶于水和水结合成硫酸,硫酸是强电解质,三氧化硫是非电解质,故C错误;
D、共价化合物只存在分子,在熔融状态下,没有离子不导电,故D正确;
故选D.
点评:本题考查了强、弱电解质的判断,抓住强弱电解质的电离程度是解答本题的关键.难度不大.

练习册系列答案
 仁爱英语同步练习册系列答案
仁爱英语同步练习册系列答案 学习实践园地系列答案
学习实践园地系列答案
相关题目
有a、b、c、d、e五种金属.已知(1)e的氧化产物比d的氧化产物氧化能力强;(2)a投入e的盐溶液中可得e的单质,而c投入e的盐溶液中却不能可得e的单质;(3)在以a、d为极板形成的原电池中(电解质溶液是稀硫酸),d极上发生还原反应;(4)电解含有a、b、c、e阳离子的盐溶液时,b离子最先在电极上放电,然后是e离子,a、c两种离子则不能在电极上放电;(5)c的单质与硫酸铜溶液反应可生产蓝色沉淀.推知五种金属的活动顺序为( )
| A、a、d、b、e、c |
| B、c、a、d、e、b |
| C、a、e、d、b、c |
| D、c、a、b、e、d |
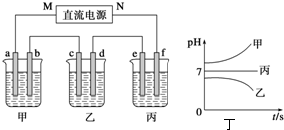
某溶液中含有两种溶质NaCl和H2SO4,它们的物质的量之比为3:1.用石墨做电极电解该混合溶液时,根据电极产物,可明显分为三个阶段,下列叙述不正确的是( )
| A、阴极自始至终只有H2 |
| B、阳极先析出Cl2后析出O2 |
| C、电解最后阶段为电解水 |
| D、溶液pH不断增大,最后为7 |
11.9g金属锡跟100mL12mol?L-1HNO3共热一段时间.完全反应后测定溶液中c(H+)为8mol?L-1,溶液体积仍为100mL.放出的气体在标准状况下体积约为8.96L.由此推断氧化产物可能是(Sn的相对原子质量为119)( )
| A、SnO2?4H2O |
| B、Sn(NO3)4 |
| C、Sn(NO3)2 |
| D、Sn(NO3)2和Sn(NO3)4 |
X、Y、Z和R为原子序数依次递增的四种元素,其中X、Y、Z属于短周期元素,X是自然界中构成化合物种类最多的元素且具有多种同素异形体,Y的最高正价是最低负价绝对值的3倍,Y、Z同周期,Z、R同主族.下列说法不正确的是( )
| A、80R的核内含有40个中子 |
| B、Y、Z、R的氢化物对应酸的酸性逐渐增强 |
| C、X、Y、R、Z单质的氧化性依次增强 |
| D、X单质与Y的最高价氧化物对应的水化物共热可生成两种气体 |
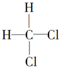 与
与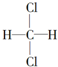 ;④
;④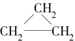 与
与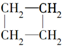
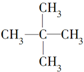 和
和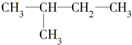 ;⑥
;⑥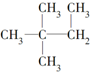 和CH3C(CH3)2CH2CH2CH3.
和CH3C(CH3)2CH2CH2CH3.