题目内容
A、B、C三种强电解质,它们在水中电离出的离子如下表所示:
如图所示装置中,甲、乙、丙三个烧杯依次分别盛放250mL足量的A溶液、足量的B溶液、足量的C溶液,电极均为石墨电极.
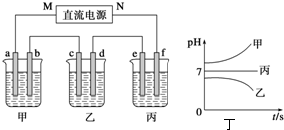
接通电源,经过一段时间后,测得乙中c电极质量增加了8g.常温下各烧杯中溶液的pH与电解时间t的关系图如图丁.据此回答下列问题:
(1)M为电源的 极(填写“正”或“负”),电极b上发生的电极反应为 .
(2)计算电极e上生成的气体在标准状况下的体积: .
(3)乙烧杯的电解反应方程式为 ;此时乙烧杯中溶液的pH= .
(4)若经过一段时间后,测得乙中c电极质量增加了m g时,要使丙恢复到原来的状态,具体操作是 .
| 阳离子 | Na+、K+、Cu2+ |
| 阴离子 | SO42-、OH- |

接通电源,经过一段时间后,测得乙中c电极质量增加了8g.常温下各烧杯中溶液的pH与电解时间t的关系图如图丁.据此回答下列问题:
(1)M为电源的
(2)计算电极e上生成的气体在标准状况下的体积:
(3)乙烧杯的电解反应方程式为
(4)若经过一段时间后,测得乙中c电极质量增加了m g时,要使丙恢复到原来的状态,具体操作是
考点:电解原理,常见离子的检验方法
专题:
分析:测得乙中c电极质量增加了8g,则乙中含有Cu2+,结合离子的共存可知,B为CuSO4,丙中pH不变,则C为硫酸钠或硫酸钾,甲中pH增大,则A为KOH或NaOH,
(1)乙中c电极铜离子得电子,则c为阴极,即M为电源负极,则b为阳极,碱溶液中OH-放电;
(2)e电极上氢离子放电生成氢气,利用Cu~2e-~H2↑来计算;
(3)乙烧杯中为惰性电极电解硫酸铜溶液;根据氢离子浓度计算PH;
(4)丙中电解质为硫酸钠或硫酸钾,实质为电解水.
(1)乙中c电极铜离子得电子,则c为阴极,即M为电源负极,则b为阳极,碱溶液中OH-放电;
(2)e电极上氢离子放电生成氢气,利用Cu~2e-~H2↑来计算;
(3)乙烧杯中为惰性电极电解硫酸铜溶液;根据氢离子浓度计算PH;
(4)丙中电解质为硫酸钠或硫酸钾,实质为电解水.
解答:
解:测得乙中c电极质量增加了8g,则乙中含有Cu2+,结合离子的共存可知,B为CuSO4,丙中pH不变,则C为硫酸钠或硫酸钾,甲中pH增大,则A为KOH或NaOH,
(1)乙中c电极铜离子得电子,则c为阴极,即M为电源负极,则b为阳极,碱溶液中OH-放电,电极反应为4OH--4e-=O2↑+2H2O,故答案为:负;4OH--4e-=O2↑+2H2O;
(2)e电极上氢离子放电生成氢气,n(Cu)=
=0.125mol,由Cu~2e-~H2↑可知生成标况下氢气的体积为0.125mol×22.4L/mol=2.8L,故答案为:2.8L;
(3)乙烧杯中为惰性电极电解硫酸铜溶液,总反应为2CuSO4+2H2O
2Cu+O2↑+2H2SO4,则根据(2)n(Cu)=
=0.125mol,所以生成硫酸也为0.125mol,所以氢离子浓度为:
=1mol/L,则PH=0,故答案为:2CuSO4+2H2O
2Cu+O2↑+2H2SO4;0;
(4)丙中电解质为硫酸钠或硫酸钾,实质为电解水,由电子守恒可知H2O~2e-~Cu,则要恢复原状,加
mol×18g/mol=
m g水,故答案为:向丙烧杯中加
m g水.
(1)乙中c电极铜离子得电子,则c为阴极,即M为电源负极,则b为阳极,碱溶液中OH-放电,电极反应为4OH--4e-=O2↑+2H2O,故答案为:负;4OH--4e-=O2↑+2H2O;
(2)e电极上氢离子放电生成氢气,n(Cu)=
| 8 |
| 64 |
(3)乙烧杯中为惰性电极电解硫酸铜溶液,总反应为2CuSO4+2H2O
| ||
| 8 |
| 64 |
| 0.125×2 |
| 0.25 |
| ||
(4)丙中电解质为硫酸钠或硫酸钾,实质为电解水,由电子守恒可知H2O~2e-~Cu,则要恢复原状,加
| m |
| 64 |
| 9 |
| 32 |
| 9 |
| 32 |
点评:本题考查电解原理,明确发生的电极反应、电解反应及图象的分析是解答本题的关键,注意利用乙推出各物质及电源的正负极是解答的突破口,题目难度中等.

练习册系列答案
 夺冠金卷全能练考系列答案
夺冠金卷全能练考系列答案
相关题目
测定空气中污染物含量的一种方法是:将一定体积的空气通入吸收剂,并测定其导电能力的变化.用上述方法测定空气中氯气的含量时,导电能力变化最大的是( )
| A、H2S溶液 |
| B、KI溶液 |
| C、NaOH溶液 |
| D、Na2S溶液 |
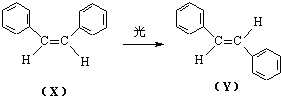 科学家经研究证实光可诱发如图所示化学变化:这一事实可解释人眼的夜视功能.有关X、Y的叙述中不正确的是( )
科学家经研究证实光可诱发如图所示化学变化:这一事实可解释人眼的夜视功能.有关X、Y的叙述中不正确的是( )| A、X和Y互为同分异构体 |
| B、X和Y都可溶于水 |
| C、X和Y都可发生加聚反应 |
| D、X和Y的所有原子都可能处于同一平面内 |
下列小实验不能制得溶液的是( )
A、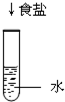 |
B、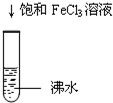 |
C、 |
D、 |
某广告称某种品牌的八宝粥(含桂圆、红豆、糯米等)不加糖,比加糖还甜,适合糖尿病人食用,你认为下列关于糖尿病人能否食用此八宝粥的判断不正确的是( )
| A、这个广告有误导喜爱甜食的消费者的嫌疑,不甜不等于没有糖 |
| B、糖尿病人应少吃含糖的食品,该八宝粥未加糖,可以放心食用 |
| C、不加糖不等于没有糖,糖尿病人食用需慎重 |
| D、不能听从厂商或广告商的宣传,应询问医生 |
下列说法正确的是( )
| A、强电解质一定是离子化合物,弱电解质一定是共价化合物 |
| B、强电解质一定是易溶化合物,弱电解质一定是难溶化合物 |
| C、SO3溶于水后水溶液导电性很强,所以SO3是强电解质 |
| D、属于共价化合物的电解质在熔化状态下一般不导电 |
从我国西部开采的天然气,通过西气东输工程供给江苏.天然气的主要成分是( )
| A、甲烷 | B、氢气 |
| C、一氧化碳 | D、乙烯 |
在25℃、101KPa下,1g甲醇燃烧生成CO2和液态水时放热22.68KJ,下列热化学方程正确的是( )
A、CH3OH(l)+
| ||
| B、2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l)△H=-1452KJ/mol | ||
C、CH3OH(l)+
| ||
| D、2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g)△H=-1452KJ/mol |