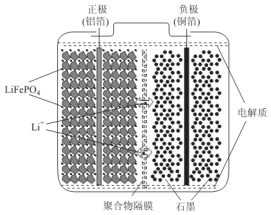
题目内容
10.为证明某可溶性一元酸(HX)是弱酸,有如下实验方案,其中不合理的是( )| A. | 室温下,测0.1 mol/L HX溶液的pH,若pH>1,证明HX是弱酸 | |
| B. | 相同条件下,对0.1 mol/L的HCl和0.1 mol/L的HX进行导电性实验,若与HX溶液相串联的灯泡较暗,证明HX为弱酸 | |
| C. | 将等浓度、等体积的HCl和NaX溶液混合,若混合溶液pH<7,证明HX是弱酸 | |
| D. | 室温下,测1 mol/L NaX溶液的pH,若pH>7,证明HX是弱酸 |
分析 要证明一元酸HX为弱酸,可证明存在电离平衡、不能完全电离或从对应的强碱盐溶液呈碱性的角度.
解答 解:A.室温下,测0.1mol/L的HX溶液的pH,若pH>1,说明HX在水溶液里不完全电离,则证明HX是弱酸,故A不选;
B.相同条件下,对0.1mol/L的HCl和0.1mol/L的HX进行导电性实验,氯化氢是强电解质,在水溶液里完全电离,若与HX溶液相串联的灯泡较暗,说明HX在水溶液里部分电离,则能证明HX是弱酸,故B不选;
C.将等浓度、等体积的HCl和NaX溶液混合,酸的电离程度大于酸根离子的水解程度,若混合溶液pH<7,不能证明HX是弱酸,故C选;
D.室温下,测0.1mol/L的NaX溶液的pH,若pH>7,说明NaX是强碱弱酸盐,HX不完全电离,为弱电解质,所以能证明HX是弱酸,故D不选;
故选C.
点评 本题考查弱电解质的电离,侧重于弱酸的实验角度的探究,注意把握实验原理和角度,题目难度中等.

练习册系列答案
相关题目
1.下列说法错误的是( )
| A. | 用丁达尔效应可鉴别FeCl2溶液和Fe(OH)3胶体 | |
| B. | Na与NaCl在灼烧时火焰颜色相同 | |
| C. | 相同条件下,Na2CO3比NaHCO3更稳定 | |
| D. | 用氨水可鉴别MgCl2溶液和AlCl3溶液 |
1.据“北方网”报道,2004年4月15日至16日,位于重庆市江北区的天原化工总厂相继发生氯气泄漏和爆炸事故.截至记者发稿时,已有9人在事故中失踪死亡,3人受伤,15万人被紧急疏散.当人们逃离爆炸现场时,可以用浸有一定浓度的某种物质的水溶液的毛巾捂住鼻子,最适宜采用的该物质是 ( )
| A. | NaOH | B. | NaCl | C. | KBr | D. | Na2CO3 |
5.将某些化学知识用图象表示,可以收到直观、简明的效果.下列图象所表示的化学知识中,明显不正确的是( )


| A. | 稀释浓盐酸过程 | |
| B. | 向氯化铝溶液中滴加氢氧化钠溶液至过量 | |
| C. | 分散系的分类 | |
| D. | 氨水与SO2反应后溶液中的铵盐 |
19.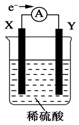 在盛有稀硫酸的烧杯中放入用导线连接的电极X、Y,外电路中电子流向如图所示,关于该装置的下列说法正确的是( )
在盛有稀硫酸的烧杯中放入用导线连接的电极X、Y,外电路中电子流向如图所示,关于该装置的下列说法正确的是( )
 在盛有稀硫酸的烧杯中放入用导线连接的电极X、Y,外电路中电子流向如图所示,关于该装置的下列说法正确的是( )
在盛有稀硫酸的烧杯中放入用导线连接的电极X、Y,外电路中电子流向如图所示,关于该装置的下列说法正确的是( )| A. | 外电路的电流方向为X→外电路→Y | |
| B. | 若两电极分别为铁和碳棒,则铁棒进行的电极反应式为2H++e-═H2↑ | |
| C. | X极上发生的是还原反应,Y极上发生的是氧化反应 | |
| D. | 若两电极都是金属,则它们的活动性顺序是X>Y |
20.下列陈述I、陈述II正确并且有因果关系的是( )
| 选项 | 陈述I | 陈述II |
| A | HC1O具有漂白性 | 湿润的Cl2能使有色布条褪色 |
| B | SiO2具有导电性 | SiO2可用于制光导纤维 |
| C | 铝的金属性比铁强 | 铝制品在空气中比铁制品更容易腐蚀 |
| D | 碳酸钠属于碱类 | 工业上的“三酸二碱”,把碳酸钠归纳为“碱” |
| A. | A | B. | B | C. | C | D. | D |
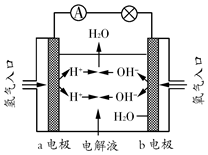 化学电池在通讯、交通及日常生活中有着广泛的应用.
化学电池在通讯、交通及日常生活中有着广泛的应用.